Si has visto todos los enlaces anteriores.Ya estás en condiciones, de poder realizar los ejercicios del tema 2. También te recuerdo que cuando os pongaís de acuerdo realizamos el examen del final del tema 1 y el del tema 2.
Me olvidaba, piensa si es tú caso en la fecha del examen de recuperación de la primera evaluación
Saludos
Este espacio está creado para los alumnos de la asignatura Ciencias Naturales de Nivel II del CEPA Torres de la Alameda
jueves, 17 de diciembre de 2009
miércoles, 16 de diciembre de 2009
CONTAMINACIÓN ATMOSFÉRICA
Se entiende por contaminación atmosférica la presencia en el aire de sustancias y formas de energía que alteran la calidad del mismo, de modo que implique riesgos, daño o molestia grave para las personas y bienes de cualquier naturaleza.
TIPOS:
la lluvia ácida
TIPOS:
la lluvia ácida
Se forma cuando la humedad en el aire se combina con los óxidos de nitrógeno y el dióxido de azufre emitidos por fábricas, centrales eléctricas y vehículos que queman carbón o productos derivados del petróleo. En interacción con el vapor de agua, estos gases forman ácido sulfúrico y ácidos nítricos. Finalmente, estas sustancias químicas caen a la tierra acompañando a las precipitaciones, constituyendo la lluvia ácida.
Formación de la lluvia ácida
Una gran parte del SO2 (dióxido de azufre) emitido a la atmósfera procede de la emisión natural que se produce por las erupciones volcánicas, que son fenómenos irregulares. Sin embargo, una de las fuentes de SO2 es la industria metalúrgica.El SO2 puede proceder también de otras fuentes, por ejemplo como el sulfuro de dimetilo, (CH3)2S, y otros derivados, o como sulfuro de hidrógeno, H2S. Estos compuestos se oxidan con el oxígeno atmosférico dando SO2.Finalmente el SO2 se oxida a SO3 (interviniendo en la reacción radicales hidroxilo y oxígeno) y este SO3 se puede quedar disuelto en las gotas de lluvia, es el de las emisiones de SO2 en procesos de obtención de energía: el carbón, el petróleo y otros combustibles fósiles contienen azufre en unas cantidades variables (generalmente más del 1%), y, debido a la combustión, el azufre se oxida a dióxidos de azufre::S + O2 → SO2Los procesos industriales en los que se genera SO2, por ejemplo son en la industria metalúrgica.En la fase gaseosa el dióxido de azufre se oxida por reacción con el radical hidroxilo por una reacción intermolecular::SO2 + OH· → HOSO2· seguida por::HOSO2· + O2 → HO2· + SO3 En presencia del agua atmosférica o sobre superficies húmedas, el trióxido de azufre (SO3) se convierte rápidamente en ácido sulfúrico::SO3(g) + H2O (l) → H2SO4(l) El NO se forma por reacción entre el oxígeno y el nitrógeno a alta temperatura::O2 + N2 → 2NOUna de las fuentes más importantes es a partir de las reacciones producidas en los motores térmicos de los automóviles y aviones, donde se alcanzan temperaturas muy altas. Este NO se oxida con el oxígeno atmosférico::O2 + 2NO → 2NO2Y este 2NO2 reacciona con el agua dando ácido nítrico que se disuelve en el agua::3NO2 + H2O → 2HNO3 + NOlunes, 14 de diciembre de 2009
REACCIONES QUÍMICAS II
Una reacción química o cambio químico es todo proceso químico en el cual dos o más sustancias (llamadas reactivos), por efecto de un factor energético, se transforman en otras sustancias llamadas productos. Esas sustancias pueden ser elementos o compuestos. Un ejemplo de reacción química es la formación de óxido de hierro producida al reaccionar el oxígeno del aire con el hierro.
A la representación simbólica de las reacciones se les llama ecuaciones químicas.
Los productos obtenidos a partir de ciertos tipos de reactivos dependen de las condiciones bajo las que se da la reacción química. No obstante, tras un estudio cuidadoso se comprueba que, aunque los productos pueden variar según cambien las condiciones, determinadas cantidades permanecen constantes en cualquier reacción química.pincha aquí
En estos enlaces se explican las ecuaciones químicas y el proceso de ajuste de las mismas.
A continuación podrás realizar ejercicios para practicar
y otros algo más difíciles
A la representación simbólica de las reacciones se les llama ecuaciones químicas.
Los productos obtenidos a partir de ciertos tipos de reactivos dependen de las condiciones bajo las que se da la reacción química. No obstante, tras un estudio cuidadoso se comprueba que, aunque los productos pueden variar según cambien las condiciones, determinadas cantidades permanecen constantes en cualquier reacción química.pincha aquí
En estos enlaces se explican las ecuaciones químicas y el proceso de ajuste de las mismas.
A continuación podrás realizar ejercicios para practicar
y otros algo más difíciles
LEY DE GAY-LUSSAC
Esta Ley indica que a una presión constante, al aumentar la temperatura, el volumen del gas aumenta y al disminuir la temperatura el volumen del gas disminuye. Esto se debe a que "temperatura" significa movimiento de las partículas. Así que, a mayor movimiento de las partículas (temperatura), mayor volumen del gas.
V1/T1= V2/T2
Mira este flash que lo explica, amí me gusta poco.
V1/T1= V2/T2
Mira este flash que lo explica, amí me gusta poco.
jueves, 10 de diciembre de 2009
LEY DE LAS PROPORCIONES MÚLTIIPLES O LEY DE DALTON
LEY DE LAS PROPORCIONES MÚLTIIPLES O LEY DE DALTON
Las investigaciones posteriores que los químicos realizaron para determinar en qué proporciones se unen los elementos químicos proporcionaron aparentes contradicciones con la ley de Proust, pues en ocasiones los elementos químicos se combinan en más de una proporción. Así, por ejemplo, 1 g de nitrógeno se puede combinar con tres proporciones distintas de oxígeno para proporcionar tres óxidos de nitrógeno diferentes, así:
Compuesto | Masa de N (g) | Masa de O (g) |
|---|---|---|
| Dióxido de nitrógeno (NO2) | 1 | 2,28 |
| Monóxido de nitrógeno (NO) | 1 | 1,14 |
| Óxido de nitrógeno (N2O) | 1 | 0,57 |
Fue John Dalton (1776-1844) quien en 1803 generalizó este hecho con numerosos compuestos, observando que cuando dos elementos se combinan entre sí para formar compuestos diferentes, las diferentes masas de uno de ellos que se combina con una masa fija de otro, guardan entre sí una relación de números enteros sencillos. De forma que en nuestro ejemplo:
2,28 / 1,14 = 2 ; 2,28 / 0,57 = 4 ; 1,14 / 0,57 = 2
LEY DE PROUST
La labor de Lavoisier proporcionó una sólida base teórica para el análisis cuantitativo y pronto surgieron los estudios que condujeron a lo que posteriormente se denomimó Ley de las Proporciones Definidas, que a finales del siglo XVIII, dio origen a una gran controversia entre Berthollet y Proust, que duró casi ocho años.
Joseph Louis Proust (1754-1826) sostenía que la composición porcentual de un compuesto químico era siempre la misma, independientemente de su origen, por el contrario Claude Louis Berthollet (1748-1822) afirmaba que los elementos, dentro de ciertos límites, podían unirse en todas las proporciones.
Con el tiempo, se impuso el criterio de Proust apoyado en un experimento realizado en 1799, demostrando que la composición del carbonato cúprico era siempre la misma, cualquiera que fuese su método de obtención en la naturaleza o en el laboratorio: 5 partes de cobre, 4 de oxígeno y 1 de carbono.
Por tanto: los elementos se combinan para formar compuestos, y siempre lo hacen en proporciones fijas y definidas.
Consecuencia de la ley de las proporciones definidas
La constitución, por ejemplo, del cloruro sódico indica que para formar 5 g de cloruro sódico, se necesitan 3 g de cloro y 2 g de sodio, por lo que la proporción entre las masas de ambos elementos es:
3 g de Cl / 2g de Na = 1,5
Sin embargo, si hacemos reaccionar ahora 10 g de cloro con otros 10 g de sodio, no obtendremos 20 g de cloruro sódico, sino una candidad menor, debido a que la relación de combinación entre ambas masas siempre es 1,5 por lo que:
3 g de Cl / 10 g de Cl = 2 g de Na / x g de Na => x = 6,6 g de Na que reaccionan
Si ahora quisiéramos hallar la proporción entre los átomos que se combinan de cloro y sodio para formar cloruro sódico, deberíamos dividir la cantidad de cada elemento entre su masa atómica, de forma que si reaccionan 6 g de Cl con 4 g de Na, como 35,5 g/mol y 23 g/mol son las masas atómicas del cloro y sodio, respectivamente, entonces:
6 g / 35,5 g/mol = 0,17 moles de Cl ; 4 g / 23 g/mol = 0,17 moles de Na
Lo que indica que por cada 0,17 moles de cloro reaccionan otros 0,17 moles de sodio para formar el cloruro sódico, o cualquier múltiplo o submúltiplo de esa reacción. Por tanto, 1 átomo de cloro también se combina con 1 átomo de sodio para formar cloruro sódico, luego la fórmula de éste compuesto es NaCl y la proporción entre sus átomos es 1:1.
LEY DE LAVOISIER
Probablemente, la aportación más importante que hizo Antonie Laurent Lavoisier (1743-1794) a la Química fue la implantación de la medida precisa a todos los procesos en los que la materia sufre transformaciones y el enunciado de la famosa ley de conservación de la masa.
En 1770 Lavoisier realizó el experimento del calentamiento del agua utilizando un aparato que condensaba el vapor y lo devolvía al recipiente, sin perder un sólo gramo de agua. Pesó el agua y el recipiente antes y después de realizar el experimento. Demostró que el peso del matráz, del condensador y del agua seguía siendo el mismo antes y después de una prolongada ebullición. Sin embargo, un sedimento terroso seguía apareciendo. Extrajo y pesó el depósito formado, así como el matráz y comprobó que la suma de ambos era igual al peso del matraz antes de iniciar la experiencia. Es decir, el poso terroso provenía de una descomposición del vidrio provocada por el calor.
Posteriormente, se ocupó de las reacciones químicas y comprobó que la masa (cantidad de materia) es algo permanente e indestructible, algo que se conserva pese a todos los cambios. Newton defendió antes en la física la idea de una masa que permanecía constante a través de todos los movimientos, y Lavoisier la aplicó al mundo de la química.
En 1774 Lavoisier enunció su ley de conservación de la masa, de forma que: en toda transformación química, la masa total de los reactivos que reaccionan es igual a la masa total de los productos de la reacción.
Así, según Lavoisier, en la reacción del cobre con el azufre para originar sulfuro cúprico, mediante:
Cu + S ® CuS
resulta que 4,00 g de Cu reaccionan con 2,02 g de S y producen 6,02 g de CuS.
Es decir, que: en una reacción química, la materia ni se crea ni se destruye, sólo se reorganiza.
Lavoisier comprobó su ley en numerosas reacciones, la mayoría de las cuales consistían en someter a calentamiento diversos metales, siempre en recipientes cerrados y con una cantidad determinada de aire, pero, sobre todo, midiendo las masas de las sustancias antes y después de la reacción. Estos experimentos le llevaron, no sólo a comprobar que el oxígeno del aire se combina con los metales durante la reacción de oxidación, sino también a demostrar la conservación de la masa duranrte el proceso.
La ley de Lavoisier hizo posible la aprarición de la ecuación química. La cual se sustenta en dos pilares, uno es la ley de Lavoisier y otro es la formulación moderna de los compuestos químicos, cuyos principios sistemáticos se deben a un conjunto de notables químicos, entre los cuales también destaca Lavoisier
Si quieres saber más
Si quieres saber más
REACCIONES QUÍMICAS
Una reacción química o cambio químico es todo proceso químico en el cual dos o más sustancias (llamadas reactivos), por efecto de un factor energético, se transforman en otras sustancias llamadas productos. Esas sustancias pueden ser elementos o compuestos. Un ejemplo de reacción química es la formación de óxido de hierro producida al reaccionar el oxígeno del aire con el hierro.
Velocidad de reacción La rapidez (o velocidad) de reacción se define como la cantidad de reactivos que se transforma o el producto que se forma por unidad de tiempo.
Catalizadores: los catalizadores son sustancias que modifican la rapidez de una reacción sin sufrir cambio aparente en su composicion o en su peso.
La energía de activación ( ) en química y biología es la energía que necesita un sistema antes de poder iniciar un determinado proceso. La energía de activación suele utilizarse para denominar la energía mínima necesaria para que se produzca una reacción química dada. Para que ocurra una reacción entre dos moléculas, éstas deben colisionar en la orientación correcta y poseer una cantidad de energía mínima. A medida que las moléculas se aproximan, sus nubes de electrones se repelen. Esto requiere energía (energía de activación) y proviene del calor del sistema, es decir de la energía traslacional, vibracional, etcétera de cada molécula. Si la energía es suficiente, se vence la repulsión y las moléculas se aproximan lo suficiente para que se produzca una reordenación de los enlaces de las moléculas.
) en química y biología es la energía que necesita un sistema antes de poder iniciar un determinado proceso. La energía de activación suele utilizarse para denominar la energía mínima necesaria para que se produzca una reacción química dada. Para que ocurra una reacción entre dos moléculas, éstas deben colisionar en la orientación correcta y poseer una cantidad de energía mínima. A medida que las moléculas se aproximan, sus nubes de electrones se repelen. Esto requiere energía (energía de activación) y proviene del calor del sistema, es decir de la energía traslacional, vibracional, etcétera de cada molécula. Si la energía es suficiente, se vence la repulsión y las moléculas se aproximan lo suficiente para que se produzca una reordenación de los enlaces de las moléculas.
Velocidad de reacción La rapidez (o velocidad) de reacción se define como la cantidad de reactivos que se transforma o el producto que se forma por unidad de tiempo.
Catalizadores: los catalizadores son sustancias que modifican la rapidez de una reacción sin sufrir cambio aparente en su composicion o en su peso.
La energía de activación (
 ) en química y biología es la energía que necesita un sistema antes de poder iniciar un determinado proceso. La energía de activación suele utilizarse para denominar la energía mínima necesaria para que se produzca una reacción química dada. Para que ocurra una reacción entre dos moléculas, éstas deben colisionar en la orientación correcta y poseer una cantidad de energía mínima. A medida que las moléculas se aproximan, sus nubes de electrones se repelen. Esto requiere energía (energía de activación) y proviene del calor del sistema, es decir de la energía traslacional, vibracional, etcétera de cada molécula. Si la energía es suficiente, se vence la repulsión y las moléculas se aproximan lo suficiente para que se produzca una reordenación de los enlaces de las moléculas.
) en química y biología es la energía que necesita un sistema antes de poder iniciar un determinado proceso. La energía de activación suele utilizarse para denominar la energía mínima necesaria para que se produzca una reacción química dada. Para que ocurra una reacción entre dos moléculas, éstas deben colisionar en la orientación correcta y poseer una cantidad de energía mínima. A medida que las moléculas se aproximan, sus nubes de electrones se repelen. Esto requiere energía (energía de activación) y proviene del calor del sistema, es decir de la energía traslacional, vibracional, etcétera de cada molécula. Si la energía es suficiente, se vence la repulsión y las moléculas se aproximan lo suficiente para que se produzca una reordenación de los enlaces de las moléculas. CAMBIOS FÍSICOS Y QUÍMICOS
Los cambios fisicos son aquellos en los cuales la materia no se transforma.. por ejemplo cuando evaporamos el agua... se transforma en vapor "de agua" con lo cual la materia no ha cambiado sigue siendo agua...
los cambios quimicos son aquellos en los que la materia se tranforma.. por ejemplo cuando quemamos un trozo de leño, este se tranforma en carbon, la materia se ha modificado.
otra forma de analizar los cambios fisicos y quimicos es por su reversibilidad... los cambios fisicos son reversibles en cambio los quimicos no... el vapor de agua se puede transformar en agua liquida pero el carbon no puede volver a ser leño.
Haz estos ejercicios de autoevaluación
los cambios quimicos son aquellos en los que la materia se tranforma.. por ejemplo cuando quemamos un trozo de leño, este se tranforma en carbon, la materia se ha modificado.
otra forma de analizar los cambios fisicos y quimicos es por su reversibilidad... los cambios fisicos son reversibles en cambio los quimicos no... el vapor de agua se puede transformar en agua liquida pero el carbon no puede volver a ser leño.
Haz estos ejercicios de autoevaluación
jueves, 26 de noviembre de 2009
TABLA PERIÓDICA 2
El día 15 de nioviembre de 2008, publique una página sobre el Sistema Periódico, podeís consultarla si os apetece, aquí pongo otro enlace sobre el mismo asunto
DIBUJO
Hemos estado viendo en clase como se puede realizar la planta el alzado y perfil de algunas figuras, en este enlace podrás ver varios ejemplos de ello . Y también construir la pieza a partir de las correspondientes vistas.Más ejemplos
Algunos ejercicios resueltos
Algunos ejercicios resueltos
martes, 17 de noviembre de 2009
DENSIDAD
La densidad es la magnitud que expresa la relación entre la masa y el volumen de un cuerpo. Su unidad en el Sistema Internacional es el kilogramo por metro cúbico (kg/m3), aunque frecuente y coloquialmente se expresa en g/cm3
Realiza las siguientes actividades para comenzar, a continuación puedes seguir con... y continua con estos ejercicios y los siguientes
Las mezclas homogéneas están formadas por una sola fase, es decir, no se pueden distinguir las partes, ni aún con la ayuda de un microscopio electrónico, presenta la misma composición en cualquiera de sus partes.
Las mezclas homogéneas se caracterizan porque físicamente no se aprecia que estén formadas por diferentes constituyentes
Si quieres ver como es el proceso de formación de una mezcla homogénea pincha aquí
Existen cinco tipos de mezclas homogéneas:
sólido - sólido (aleación)
líquido - sólido
líquido - líquido
gas - líquido
gas - sólido
Mezclas Heterogéneas son aquellas cuyo aspecto difiere de una parte a otra de ella, está formada por dos o más componentes que se distinguen a simple vista o no y contiene cantidades diferentes de los componentes. El granito, las rocas, arena y agua, la sopa de verduras, las ensaladas son ejemplos de mezclas heterogéneas.
Emulsión es una mezcla heterogénea de dos o más líquidos inmiscibles.Ejemplos Ejemplos de emulsiones incluyen la mantequilla y la margarina, la leche y la nata, la salsa mahonesa.
Suspensión es un mezcla de sólido y líquido que se pueden filtrar, ejemplo yeso en agua.
La filtración es una técnica, por la cual se hace pasar una mezcla de sólidos y fluidos, gas o líquido, a través de un medio poroso o medio filtrante que puede formar parte de un dispositivo denominado filtro, donde se retiene de la mayor parte del o de los componentes sólidos de la mezcla.
TÉCNICAS DE SEPARACIÓN DE MEZCLAS
La decantación . Se basa en la diferencia de densidad entre los dos componentes, que hace que dejados en reposo, ambos se separen hasta situarse el más denso en la parte inferior del envase que los contiene. De esta forma, podemos vaciar el contenido por arriba o por abajo en un embudo de decantación.
La destilación es la operación de separar, comúnmente mediante calor, los diferentes componentes líquidos de una mezcla, aprovechando los diferentes puntos de ebullición (temperaturas de ebullición) de cada una de las sustancias a separar.
La sedimentación es el proceso por el cual el material sólido, transportado por una corriente de agua, se deposita en el fondo del río, embalse, canal artificial, o dispositivo construido especialmente para tal fin. Toda corriente de agua, caracterizada por su caudal,
La sublimación es el proceso que consiste en el cambio de estado de la materia sólida al estado gaseoso sin pasar por el estado líquido. Se puede llamar de la misma forma al proceso inverso, el paso directo del estado gaseoso al estado sólido, pero es más apropiado referirse a esa transición como sublimación inversa. Un ejemplo clásico de sustancia capaz de sublimarse es el hielo seco.
La evaporación es el proceso físico por el cual una sustancia en estado líquido pasa al estado gaseoso, tras haber adquirido energía suficiente para vencer la tensión superficial. A diferencia de la ebullición, este proceso se produce a cualquier temperatura, siendo más rápido cuanto más elevada sea aquélla. No es necesario que toda la masa alcance el punto de ebullición.
La centrifugación es un método por el cual se pueden separar sólidos de líquidos de diferente densidad mediante una centrifugadora, la cual imprime a la mezcla un movimiento rotatorio con una fuerza de mayor intensidad que la gravedad, provocando la sedimentación del sólido o de las partículas de mayor densidad.
La adsorción es un proceso por el cual átomos, iones o moléculas son atrapadas o retenidas en la superficie de un material
La Cromatografía es una técnica que permite separar los componentes de una mezcla haciéndola pasar a través de un medio adsorbente (adhesión a una superficie). Una de las más sencillas es la cromatografía en papel que emplea como medio adsorbente papel filtro y como solvente un líquido.Los distintos componentes se separan debido a que cada uno de ellos manifiesta diferentes afinidades por el papel filtro o por el disolvente.
El Tamizado es un método de separación, es uno de los más sencillos y consiste en hacer pasar una mezcla de sólidos, de distinto tamaño, a través de un tamiz. Los granos más pequeños atraviesan el tamiz y los más grandes son retenidos.
Disolución es una mezcla homogénea, a nivel molecular de una o más especies químicas que no reaccionan entre sí; cuyos componentes se encuentran en proporción que varía entre ciertos límites.
Toda disolución está formada por una fase dispersa llamada soluto y un medio dispersante denominado disolvente. También se define solvente como la sustancia que existe en mayor cantidad que el soluto en la disolución. Si ambos, soluto y solvente, existen en igual cantidad (como un 50% de etanol y 50% de agua en una disolución), la sustancia que es más frecuentemente utilizada como solvente es la que se designa como tal (en este caso, el agua). Una disolución puede estar formada por uno o más solutos y uno o más disolventes. Una disolución será una mezcla en la misma proporción en cualquier cantidad que tomemos (por pequeña que sea la gota), y no se podrán separar por centrifugación ni filtración.
Un ejemplo común podría ser un sólido disuelto en un líquido, como la sal o el azúcar disuelto en agua.
La solubilidad es una medida de la capacidad de una determinada sustancia para disolverse en otra. Puede expresarse en moles por litro, en gramos por litro, o en porcentaje de soluto; en algunas condiciones se puede sobrepasarla, denominándose a estas soluciones sobresaturadas. El método preferido para hacer que el soluto se disuelva en esta clase de soluciones es calentar la muestra. La sustancia que se disuelve se denomina soluto y la sustancia donde se disuelve el soluto se llama disolvente. No todas las sustancias se disuelven en un mismo solvente, por ejemplo en el agua, se disuelve el alcohol y la sal. El aceite y la gasolina no se disuelven
Las mezclas homogéneas se caracterizan porque físicamente no se aprecia que estén formadas por diferentes constituyentes
Si quieres ver como es el proceso de formación de una mezcla homogénea pincha aquí
Existen cinco tipos de mezclas homogéneas:
sólido - sólido (aleación)
líquido - sólido
líquido - líquido
gas - líquido
gas - sólido
Mezclas Heterogéneas son aquellas cuyo aspecto difiere de una parte a otra de ella, está formada por dos o más componentes que se distinguen a simple vista o no y contiene cantidades diferentes de los componentes. El granito, las rocas, arena y agua, la sopa de verduras, las ensaladas son ejemplos de mezclas heterogéneas.
Emulsión es una mezcla heterogénea de dos o más líquidos inmiscibles.Ejemplos Ejemplos de emulsiones incluyen la mantequilla y la margarina, la leche y la nata, la salsa mahonesa.
Suspensión es un mezcla de sólido y líquido que se pueden filtrar, ejemplo yeso en agua.
La filtración es una técnica, por la cual se hace pasar una mezcla de sólidos y fluidos, gas o líquido, a través de un medio poroso o medio filtrante que puede formar parte de un dispositivo denominado filtro, donde se retiene de la mayor parte del o de los componentes sólidos de la mezcla.
TÉCNICAS DE SEPARACIÓN DE MEZCLAS
La decantación . Se basa en la diferencia de densidad entre los dos componentes, que hace que dejados en reposo, ambos se separen hasta situarse el más denso en la parte inferior del envase que los contiene. De esta forma, podemos vaciar el contenido por arriba o por abajo en un embudo de decantación.
La destilación es la operación de separar, comúnmente mediante calor, los diferentes componentes líquidos de una mezcla, aprovechando los diferentes puntos de ebullición (temperaturas de ebullición) de cada una de las sustancias a separar.
La sedimentación es el proceso por el cual el material sólido, transportado por una corriente de agua, se deposita en el fondo del río, embalse, canal artificial, o dispositivo construido especialmente para tal fin. Toda corriente de agua, caracterizada por su caudal,
La sublimación es el proceso que consiste en el cambio de estado de la materia sólida al estado gaseoso sin pasar por el estado líquido. Se puede llamar de la misma forma al proceso inverso, el paso directo del estado gaseoso al estado sólido, pero es más apropiado referirse a esa transición como sublimación inversa. Un ejemplo clásico de sustancia capaz de sublimarse es el hielo seco.
La evaporación es el proceso físico por el cual una sustancia en estado líquido pasa al estado gaseoso, tras haber adquirido energía suficiente para vencer la tensión superficial. A diferencia de la ebullición, este proceso se produce a cualquier temperatura, siendo más rápido cuanto más elevada sea aquélla. No es necesario que toda la masa alcance el punto de ebullición.
La centrifugación es un método por el cual se pueden separar sólidos de líquidos de diferente densidad mediante una centrifugadora, la cual imprime a la mezcla un movimiento rotatorio con una fuerza de mayor intensidad que la gravedad, provocando la sedimentación del sólido o de las partículas de mayor densidad.
La adsorción es un proceso por el cual átomos, iones o moléculas son atrapadas o retenidas en la superficie de un material
La Cromatografía es una técnica que permite separar los componentes de una mezcla haciéndola pasar a través de un medio adsorbente (adhesión a una superficie). Una de las más sencillas es la cromatografía en papel que emplea como medio adsorbente papel filtro y como solvente un líquido.Los distintos componentes se separan debido a que cada uno de ellos manifiesta diferentes afinidades por el papel filtro o por el disolvente.
El Tamizado es un método de separación, es uno de los más sencillos y consiste en hacer pasar una mezcla de sólidos, de distinto tamaño, a través de un tamiz. Los granos más pequeños atraviesan el tamiz y los más grandes son retenidos.
Disolución es una mezcla homogénea, a nivel molecular de una o más especies químicas que no reaccionan entre sí; cuyos componentes se encuentran en proporción que varía entre ciertos límites.
Toda disolución está formada por una fase dispersa llamada soluto y un medio dispersante denominado disolvente. También se define solvente como la sustancia que existe en mayor cantidad que el soluto en la disolución. Si ambos, soluto y solvente, existen en igual cantidad (como un 50% de etanol y 50% de agua en una disolución), la sustancia que es más frecuentemente utilizada como solvente es la que se designa como tal (en este caso, el agua). Una disolución puede estar formada por uno o más solutos y uno o más disolventes. Una disolución será una mezcla en la misma proporción en cualquier cantidad que tomemos (por pequeña que sea la gota), y no se podrán separar por centrifugación ni filtración.
Un ejemplo común podría ser un sólido disuelto en un líquido, como la sal o el azúcar disuelto en agua.
La solubilidad es una medida de la capacidad de una determinada sustancia para disolverse en otra. Puede expresarse en moles por litro, en gramos por litro, o en porcentaje de soluto; en algunas condiciones se puede sobrepasarla, denominándose a estas soluciones sobresaturadas. El método preferido para hacer que el soluto se disuelva en esta clase de soluciones es calentar la muestra. La sustancia que se disuelve se denomina soluto y la sustancia donde se disuelve el soluto se llama disolvente. No todas las sustancias se disuelven en un mismo solvente, por ejemplo en el agua, se disuelve el alcohol y la sal. El aceite y la gasolina no se disuelven
jueves, 5 de noviembre de 2009
MASA MOLECULAR
Masa molecular
La masa molecular se calcula sumando las masas atómicas de los elementos que componen la moléculaEn el caso de la molécula de agua, H2O, su masa molecular sería:
- 2X1 +16=18
(Se multiplica por 2, ya que ésa es la cantidad de veces que el elemento H está presente en la molécula.)
Aquí tienes más información
ENLACES QUÍMICOS
Cuándo hacemos leche en polvo, o cuando le echamos azúcar al té, ¿desaparece la leche o el azúcar? Claro que no, uno respondería que estos se están disolviendo en el agua. Pero en realidad, ¿Qué sucede? ¿Por qué sucede? Son hechos tan comunes que se nos olvida hacernos estas preguntas. En realidad lo que sucede es que la leche y el azúcar son solutos, que serán disueltos en un solvente como el agua. Pero ¿qué es lo que en realidad sucede? ¿Qué son los solutos y los solventes? Bueno estas preguntas serán respondidas en este informe.
Este informe habla de enlaces y soluciones, pero, para entenderlos hay que empezar por conocer el significado de estas palabras, para luego poder pasar a un lenguaje más técnico. Enlace significa unión, un enlace químico es la unión de dos o más átomos que se han unido con un solo fin, alcanzar la estabilidad, tratar de parecerse al gas noble más cercano, para la mayoría de los elementos alcanzar ocho electrones en su último nivel. Las soluciones son mezclas homogéneas, no se distinguen sus componentes como separados, entre al menos dos reactantes un soluto, que es él que será disuelto, y un solvente, que es él que disolverá al soluto. A continuación tienes unos ejercicios que puedes realizar .Te pedira una contraseña, no hagas caso, cierra la ventanita y continua.
Este informe habla de enlaces y soluciones, pero, para entenderlos hay que empezar por conocer el significado de estas palabras, para luego poder pasar a un lenguaje más técnico. Enlace significa unión, un enlace químico es la unión de dos o más átomos que se han unido con un solo fin, alcanzar la estabilidad, tratar de parecerse al gas noble más cercano, para la mayoría de los elementos alcanzar ocho electrones en su último nivel. Las soluciones son mezclas homogéneas, no se distinguen sus componentes como separados, entre al menos dos reactantes un soluto, que es él que será disuelto, y un solvente, que es él que disolverá al soluto. A continuación tienes unos ejercicios que puedes realizar .Te pedira una contraseña, no hagas caso, cierra la ventanita y continua.
sábado, 31 de octubre de 2009
ATOMOS Y COMPAÑIA
Definición de átomo pincha en el enlace anterior y podrás conocer toda la teoría atómica y su historia.
A continuación tienes un enlace a diversas actividades sobre el tema
http://concurso.cnice.mec.es/cnice2005/93_iniciacion_interactiva_materia/curso/materiales/atomo/modelos.htm
¡¡QUE TE DIVIERTAS!!
A continuación tienes un enlace a diversas actividades sobre el tema
http://concurso.cnice.mec.es/cnice2005/93_iniciacion_interactiva_materia/curso/materiales/atomo/modelos.htm
¡¡QUE TE DIVIERTAS!!
TABLA PERIÓDICA DE LOS ELEMENTOS
La tabla periódica de los elementos fue propuesta por Dimitri Mendeleiev y Julius Lothar Meyer quienes, trabajando por separado, prepararon una ordenación de todos los 64 elementos conocidos, basándose en la variación de las propiedades químicas (Mendeleiev) y físicas (Meyer) con la variación de sus masas atómicas. En la Tabla periódica de Mendeleiev los periodos (filas diagonales y oblicuas) no tenían siempre la misma longitud, pero a lo largo de los mismos había una variación gradual de las propiedades, de tal forma que los elementos de un mismo grupo o familia se correspondían en los diferentes periodos. Esta tabla fue publicada en 1869, sobre la base de que las propiedades de los elementos son función periódica de sus pesos atómicos.
Para saber más sobre la Tabla Periódica
Para saber más sobre la Tabla Periódica
martes, 27 de octubre de 2009
sábado, 10 de octubre de 2009
CONCENTRACIÓN
En química, la concentración de una disolución es la proporción o relación que hay entre la cantidad de soluto y la cantidad de disolvente, donde el soluto es la sustancia que se disuelve, el disolvente la sustancia que disuelve al soluto, y la disolución es el resultado de la mezcla homogénea de las dos anteriores. A menor proporción de soluto disuelto en el disolvente, menos concentrada está la disolución, y a mayor proporción más concentrada es ésta.
El alcohol comercial de uso doméstico, por ejemplo, generalmente no viene en una presentación pura (100% alcohol), sino que es una disolución de alcohol en agua en cierta proporción, donde el alcohol es el soluto (la sustancia que se disuelve) y el agua es el disolvente (la sustancia que disuelve el soluto). Cuando la etiqueta del envase dice que este alcohol está al 70% V/V (de concentración) significa que hay un 70% de alcohol, y el resto, el 30%, es agua.
Concentración en términos cualitativos
La concentración de las disoluciones en términos cualitativos, también llamados empíricos, no toma en cuenta cuantitativamente (numéricamente) la cantidad exacta de soluto y disolvente presentes, y dependiendo de su proporción la concentración se clasifica como sigue:
Dependiendo de la proporción de soluto con respecto al disolvente, una disolución puede estar diluida o concentrada:
El alcohol comercial de uso doméstico, por ejemplo, generalmente no viene en una presentación pura (100% alcohol), sino que es una disolución de alcohol en agua en cierta proporción, donde el alcohol es el soluto (la sustancia que se disuelve) y el agua es el disolvente (la sustancia que disuelve el soluto). Cuando la etiqueta del envase dice que este alcohol está al 70% V/V (de concentración) significa que hay un 70% de alcohol, y el resto, el 30%, es agua.
Concentración en términos cualitativos
La concentración de las disoluciones en términos cualitativos, también llamados empíricos, no toma en cuenta cuantitativamente (numéricamente) la cantidad exacta de soluto y disolvente presentes, y dependiendo de su proporción la concentración se clasifica como sigue:Diluida o concentrada
A menudo en el lenguaje informal, no técnico, la concentración se describe de una manera cualitativa, con el uso de adjetivos como "diluido" o "débil" para las disoluciones de concentración relativamente baja, y de otros como "concentrado" o "fuerte" para las disoluciones de concentración relativamente alta. En una mezcla, esos términos relacionan la cantidad de una sustancia con la intensidad observable de los efectos o propiedades, como el color, sabor, olor, viscosidad, conductividad eléctrica, etc, causados por esa sustancia. Por ejemplo, la concentración de un café puede determinarse por la intensidad de su color y sabor, la de una limonada por su sabor y olor, la del agua azucarada por su sabor. Una regla práctica es que cuanto más concentrada es una disolución cromática, generalmente más intensamente coloreada está.Dependiendo de la proporción de soluto con respecto al disolvente, una disolución puede estar diluida o concentrada:
- Disolución diluida: Es aquella en donde la cantidad de soluto está en una pequeña proporción en un volumen determinado.
- Disolución concentrada: Es la que tiene una cantidad considerable de soluto en un volumen determinado. Las soluciones saturadas y sobresaturadas son altamente concentradas.
Formas de expresar la concentración (de momento, luego habrá más)
Formas de expresar la concentración (de momento, luego habrá más)
Gramos por litro
Indica la masa en gramos disuelta en cada litro de disolución. Tiene la ventaja de ser una concentración expresada en unidades directamente medibles para el tipo de disoluciones más frecuentes en química (las de sólidos en líquidos). La balanza expresa la medida de la masa de soluto en gramos y los recipientes de uso habitual en química indican el volumen de líquido contenido en litros o en sus submúltiplos. Su cálculo es, pues, inmediato: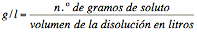
Tanto por ciento en peso
Expresa la masa en gramos de soluto disuelta por cada cien gramos de disolución. Su cálculo requiere considerar separadamente la masa del soluto y la del disolvente: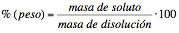
siendo la masa de la disolución la suma de la del soluto y la del disolvente.
Aplicación: cálculo de concentraciones
Se mezclan 5,00 g de cloruro de hidrógeno (HCI) con 35,00 g de agua, formándose una disolución cuya densidad a 20 ºC es de 1,060 g/cm3. Calcúlese: a) El tanto por ciento en peso, y b) La concentración en gramos por litro.a) Tanto por ciento.
Se trata de calcular el número de gramos de soluto por cada cien gramos de disolución, es decir:b) Gramos/litro.
Puesto que los datos están referidos a masas y no a volúmenes, es necesario recurrir al valor de la densidad y proceder del siguiente modo:1. Se calcula la masa de un litro de disolución:
masa = volumen · densidad = 1.000 cm3 · 1,060 g/cm3 = 1.060 g
2. A partir del valor del tanto por ciento en peso se determina la masa en gramos del soluto contenida en la disolución:
La cantidad resultante representa la concentración en gramos de soluto (HCI) por litro de disolución.
ejercicios de disoluciones
domingo, 4 de octubre de 2009
TIPOS DE MEZCLAS
Las mezclas homogéneas están formadas por una sola fase, es decir, no se pueden distinguir las partes, ni aún con la ayuda de un microscopio electrónico, presenta la misma composición en cualquiera de sus partes.
Las mezclas homogéneas se caracterizan porque físicamente no se aprecia que estén formadas por diferentes constituyentes
Si quieres ver como es el proceso de formación de una mezcla homogénea pincha aquí
Existen cinco tipos de mezclas homogéneas:
sólido - sólido (aleación)
líquido - sólido (disolución)
líquido - líquido
gas - líquido
gas - gas
Mezclas Heterogéneas son aquellas cuyo aspecto difiere de una parte a otra de ella, está formada por dos o más componentes que se distinguen a simple vista o no y contiene cantidades diferentes de los componentes. El granito, las rocas, arena y agua, la sopa de verduras, las ensaladas son ejemplos de mezclas heterogéneas.
Emulsión es una mezcla heterogénea de dos o más líquidos inmiscibles.Ejemplos Ejemplos de emulsiones incluyen la mantequilla y la margarina, la leche y la nata, la salsa mahonesa.
Suspensión es un mezcla de sólido y líquido que se pueden filtrar, ejemplo yeso en agua.
La filtración es una técnica, por la cual se hace pasar una mezcla de sólidos y fluidos, gas o líquido, a través de un medio poroso o medio filtrante que puede formar parte de un dispositivo denominado filtro, donde se retiene de la mayor parte del o de los componentes sólidos de la mezcla.
TÉCNICAS DE SEPARACIÓN DE MEZCLAS
La decantación . Se basa en la diferencia de densidad entre los dos componentes, que hace que dejados en reposo, ambos se separen hasta situarse el más denso en la parte inferior del envase que los contiene. De esta forma, podemos vaciar el contenido por arriba o por abajo en un embudo de decantación.
La destilación es la operación de separar, comúnmente mediante calor, los diferentes componentes líquidos de una mezcla, aprovechando los diferentes puntos de ebullición (temperaturas de ebullición) de cada una de las sustancias a separar.
La sedimentación es el proceso por el cual el material sólido, transportado por una corriente de agua, se deposita en el fondo del río, embalse, canal artificial, o dispositivo construido especialmente para tal fin. Toda corriente de agua, caracterizada por su caudal,
La sublimación es el proceso que consiste en el cambio de estado de la materia sólida al estado gaseoso sin pasar por el estado líquido. Se puede llamar de la misma forma al proceso inverso, el paso directo del estado gaseoso al estado sólido, pero es más apropiado referirse a esa transición como sublimación inversa. Un ejemplo clásico de sustancia capaz de sublimarse es el hielo seco.
La evaporación es el proceso físico por el cual una sustancia en estado líquido pasa al estado gaseoso, tras haber adquirido energía suficiente para vencer la tensión superficial. A diferencia de la ebullición, este proceso se produce a cualquier temperatura, siendo más rápido cuanto más elevada sea aquélla. No es necesario que toda la masa alcance el punto de ebullición.
La centrifugación es un método por el cual se pueden separar sólidos de líquidos de diferente densidad mediante una centrifugadora, la cual imprime a la mezcla un movimiento rotatorio con una fuerza de mayor intensidad que la gravedad, provocando la sedimentación del sólido o de las partículas de mayor densidad.
La adsorción es un proceso por el cual átomos, iones o moléculas son atrapadas o retenidas en la superficie de un material
La Cromatografía es una técnica que permite separar los componentes de una mezcla haciéndola pasar a través de un medio adsorbente (adhesión a una superficie). Una de las más sencillas es la cromatografía en papel que emplea como medio adsorbente papel filtro y como solvente un líquido.Los distintos componentes se separan debido a que cada uno de ellos manifiesta diferentes afinidades por el papel filtro o por el disolvente.
El Tamizado es un método de separación, es uno de los más sencillos y consiste en hacer pasar una mezcla de sólidos, de distinto tamaño, a través de un tamiz. Los granos más pequeños atraviesan el tamiz y los más grandes son retenidos.
Disolución es una mezcla homogénea, a nivel molecular de una o más especies químicas que no reaccionan entre sí; cuyos componentes se encuentran en proporción que varía entre ciertos límites.
Toda disolución está formada por una fase dispersa llamada soluto y un medio dispersante denominado disolvente. También se define solvente como la sustancia que existe en mayor cantidad que el soluto en la disolución. Si ambos, soluto y solvente, existen en igual cantidad (como un 50% de etanol y 50% de agua en una disolución), la sustancia que es más frecuentemente utilizada como solvente es la que se designa como tal (en este caso, el agua). Una disolución puede estar formada por uno o más solutos y uno o más disolventes. Una disolución será una mezcla en la misma proporción en cualquier cantidad que tomemos (por pequeña que sea la gota), y no se podrán separar por centrifugación ni filtración.
Un ejemplo común podría ser un sólido disuelto en un líquido, como la sal o el azúcar disuelto en agua.
La solubilidad es una medida de la capacidad de una determinada sustancia para disolverse en otra. Puede expresarse en moles por litro, en gramos por litro, o en porcentaje de soluto; en algunas condiciones se puede sobrepasarla, denominándose a estas soluciones sobresaturadas. El método preferido para hacer que el soluto se disuelva en esta clase de soluciones es calentar la muestra. La sustancia que se disuelve se denomina soluto y la sustancia donde se disuelve el soluto se llama disolvente. No todas las sustancias se disuelven en un mismo solvente, por ejemplo en el agua, se disuelve el alcohol y la sal. El aceite y la gasolina no se disuelven
Las mezclas homogéneas se caracterizan porque físicamente no se aprecia que estén formadas por diferentes constituyentes
Si quieres ver como es el proceso de formación de una mezcla homogénea pincha aquí
Existen cinco tipos de mezclas homogéneas:
sólido - sólido (aleación)
líquido - sólido (disolución)
líquido - líquido
gas - líquido
gas - gas
Mezclas Heterogéneas son aquellas cuyo aspecto difiere de una parte a otra de ella, está formada por dos o más componentes que se distinguen a simple vista o no y contiene cantidades diferentes de los componentes. El granito, las rocas, arena y agua, la sopa de verduras, las ensaladas son ejemplos de mezclas heterogéneas.
Emulsión es una mezcla heterogénea de dos o más líquidos inmiscibles.Ejemplos Ejemplos de emulsiones incluyen la mantequilla y la margarina, la leche y la nata, la salsa mahonesa.
Suspensión es un mezcla de sólido y líquido que se pueden filtrar, ejemplo yeso en agua.
La filtración es una técnica, por la cual se hace pasar una mezcla de sólidos y fluidos, gas o líquido, a través de un medio poroso o medio filtrante que puede formar parte de un dispositivo denominado filtro, donde se retiene de la mayor parte del o de los componentes sólidos de la mezcla.
TÉCNICAS DE SEPARACIÓN DE MEZCLAS
La decantación . Se basa en la diferencia de densidad entre los dos componentes, que hace que dejados en reposo, ambos se separen hasta situarse el más denso en la parte inferior del envase que los contiene. De esta forma, podemos vaciar el contenido por arriba o por abajo en un embudo de decantación.
La destilación es la operación de separar, comúnmente mediante calor, los diferentes componentes líquidos de una mezcla, aprovechando los diferentes puntos de ebullición (temperaturas de ebullición) de cada una de las sustancias a separar.
La sedimentación es el proceso por el cual el material sólido, transportado por una corriente de agua, se deposita en el fondo del río, embalse, canal artificial, o dispositivo construido especialmente para tal fin. Toda corriente de agua, caracterizada por su caudal,
La sublimación es el proceso que consiste en el cambio de estado de la materia sólida al estado gaseoso sin pasar por el estado líquido. Se puede llamar de la misma forma al proceso inverso, el paso directo del estado gaseoso al estado sólido, pero es más apropiado referirse a esa transición como sublimación inversa. Un ejemplo clásico de sustancia capaz de sublimarse es el hielo seco.
La evaporación es el proceso físico por el cual una sustancia en estado líquido pasa al estado gaseoso, tras haber adquirido energía suficiente para vencer la tensión superficial. A diferencia de la ebullición, este proceso se produce a cualquier temperatura, siendo más rápido cuanto más elevada sea aquélla. No es necesario que toda la masa alcance el punto de ebullición.
La centrifugación es un método por el cual se pueden separar sólidos de líquidos de diferente densidad mediante una centrifugadora, la cual imprime a la mezcla un movimiento rotatorio con una fuerza de mayor intensidad que la gravedad, provocando la sedimentación del sólido o de las partículas de mayor densidad.
La adsorción es un proceso por el cual átomos, iones o moléculas son atrapadas o retenidas en la superficie de un material
La Cromatografía es una técnica que permite separar los componentes de una mezcla haciéndola pasar a través de un medio adsorbente (adhesión a una superficie). Una de las más sencillas es la cromatografía en papel que emplea como medio adsorbente papel filtro y como solvente un líquido.Los distintos componentes se separan debido a que cada uno de ellos manifiesta diferentes afinidades por el papel filtro o por el disolvente.
El Tamizado es un método de separación, es uno de los más sencillos y consiste en hacer pasar una mezcla de sólidos, de distinto tamaño, a través de un tamiz. Los granos más pequeños atraviesan el tamiz y los más grandes son retenidos.
Disolución es una mezcla homogénea, a nivel molecular de una o más especies químicas que no reaccionan entre sí; cuyos componentes se encuentran en proporción que varía entre ciertos límites.
Toda disolución está formada por una fase dispersa llamada soluto y un medio dispersante denominado disolvente. También se define solvente como la sustancia que existe en mayor cantidad que el soluto en la disolución. Si ambos, soluto y solvente, existen en igual cantidad (como un 50% de etanol y 50% de agua en una disolución), la sustancia que es más frecuentemente utilizada como solvente es la que se designa como tal (en este caso, el agua). Una disolución puede estar formada por uno o más solutos y uno o más disolventes. Una disolución será una mezcla en la misma proporción en cualquier cantidad que tomemos (por pequeña que sea la gota), y no se podrán separar por centrifugación ni filtración.
Un ejemplo común podría ser un sólido disuelto en un líquido, como la sal o el azúcar disuelto en agua.
La solubilidad es una medida de la capacidad de una determinada sustancia para disolverse en otra. Puede expresarse en moles por litro, en gramos por litro, o en porcentaje de soluto; en algunas condiciones se puede sobrepasarla, denominándose a estas soluciones sobresaturadas. El método preferido para hacer que el soluto se disuelva en esta clase de soluciones es calentar la muestra. La sustancia que se disuelve se denomina soluto y la sustancia donde se disuelve el soluto se llama disolvente. No todas las sustancias se disuelven en un mismo solvente, por ejemplo en el agua, se disuelve el alcohol y la sal. El aceite y la gasolina no se disuelven
CAMBIOS DE ESTADO
En física y química se denomina cambio de estado a la evolución de la materia entre varios estados de agregación sin que ocurra un cambio en su composición. Los tres estados básicos son el sólido, el líquido y el gaseoso.
La siguiente tabla indica cómo se denominan los cambios de estado:
También se puede ver claramente con el siguiente gráfico:
Los dos parámetros de los que depende que una sustancia o mezcla se encuentre en un estado o en otro son temperatura y presión. La temperatura es una medida de la energía cinética de las moléculas y átomos de un cuerpo. Un aumento de temperatura o una reducción de la presión favorecen la fusión, la evaporación y la sublimación, mientras que un descenso de temperatura o un aumento de presión favorecen los cambios opuestos.
La teoría cinética explica el por qué de los cambios de estado de una sustancia. La respuesta está en el calentamiento o enfriamiento al que debe ser sometida dicha sustancia.
Al calentar la sustacia la agitación de las partículas es mucho mayor por lo que sube la temperatura, de forma que si la sustancia es sólida la sustancia puede pasar de sólido a líquido a gas, dependiendo del grado de agitación de las partículas y así facilitar la fusión, vaporización o sublimación.
Por el contario al enfriar dicha sustancia la agitación de las partículas disminuye y permite realizar los cambios de estado inversos: solidificación, licuación o condensación, sublimación regresiva.
En ninguno de los cambios de estado las paríiculas se quedan quietas. Cuando las partículas están en estado sólido vibran, cuando reciben energía en forma de calor aumenta la energía de las vibraciones lo que produce un aumento de temperatura. Llega un momento en el que la vibración es tan alta que vence las fuerzas que mantienen juntas a las partículas, y así se da el cambio de estado. De igual forma sucede con el cambio de estado de líquido a gaseoso.
El calor latente depende de algunos datos:
- La masa (m) de dicha sustancia. - Cantidad de calor Q.
La formula es:
La siguiente tabla indica cómo se denominan los cambios de estado:
| Inicial\Final | Sólido | Líquido | Gas |
|---|---|---|---|
| Sólido | fusión | Sublimación, sublimación progresiva o sublimación directa | |
| Líquido | solidificación | evaporación o ebullición | |
| Gas | sublimación inversa, regresiva o deposición | condensación y licuefacción (Licuación) |
También se puede ver claramente con el siguiente gráfico:
Los dos parámetros de los que depende que una sustancia o mezcla se encuentre en un estado o en otro son temperatura y presión. La temperatura es una medida de la energía cinética de las moléculas y átomos de un cuerpo. Un aumento de temperatura o una reducción de la presión favorecen la fusión, la evaporación y la sublimación, mientras que un descenso de temperatura o un aumento de presión favorecen los cambios opuestos.
- la fusión es el cambio de estado de sólido a líquido. Por el contrario la solidificación es el cambio inverso, de líquido a sólido.
- La vaporización es el cambio de estado de líquido a gas. Contrariamente la licuación o condensación es el cambio inverso, de gas a líquido.
- La sublimación es el cambio de estado de sólido a gas, y el cambio inverso recibe el nombre de sublimación regresiva.
La teoría cinética explica el por qué de los cambios de estado de una sustancia. La respuesta está en el calentamiento o enfriamiento al que debe ser sometida dicha sustancia.
Al calentar la sustacia la agitación de las partículas es mucho mayor por lo que sube la temperatura, de forma que si la sustancia es sólida la sustancia puede pasar de sólido a líquido a gas, dependiendo del grado de agitación de las partículas y así facilitar la fusión, vaporización o sublimación.
Por el contario al enfriar dicha sustancia la agitación de las partículas disminuye y permite realizar los cambios de estado inversos: solidificación, licuación o condensación, sublimación regresiva.
En ninguno de los cambios de estado las paríiculas se quedan quietas. Cuando las partículas están en estado sólido vibran, cuando reciben energía en forma de calor aumenta la energía de las vibraciones lo que produce un aumento de temperatura. Llega un momento en el que la vibración es tan alta que vence las fuerzas que mantienen juntas a las partículas, y así se da el cambio de estado. De igual forma sucede con el cambio de estado de líquido a gaseoso.
- El calor necesario para que se produzca el cambio de estado de una sustancia se llama calo latente (L)
El calor latente depende de algunos datos:
- La masa (m) de dicha sustancia. - Cantidad de calor Q.
La formula es:
Q=m.L
ESTADOS DE AGREGACIÓN
Estados de agregación
La materia se nos presenta en muchas fases o estados, todos con propiedades y características diferentes, y aunque los más conocidos y observables cotidianamente son tres:
La materia se nos presenta en muchas fases o estados, todos con propiedades y características diferentes, y aunque los más conocidos y observables cotidianamente son tres:
DENSIDAD
La densidad es la magnitud que expresa la relación entre la masa y el volumen de un cuerpo.
d= masa/volumen
Su unidad en el Sistema Internacional es el kilogramo por metro cúbico (kg/m3), aunque frecuente y coloquialmente se expresa en g/cm3
Unidades de densidad
- kilogramo por metro cúbico (kg/m³).
- gramo por centímetro cúbico (g/cm³).
Sustancia Densidad en kg/m3 Densidad en g/cm3
Agua 1000 1
Aceite 920 0,92
Gasolina 680 0,68
Plomo 11300 11,3
Acero 7800 7,8
Mercurio 13600 13,6
Madera 900 0,9
Aire 1,3 0,0013
Butano 2,6 0,026
Dióxido de carbono 1,8 0,018
Puedes continuar con estos otros
o estos
miércoles, 30 de septiembre de 2009
SISTEMAS MATERIALES
Materia es todo aquello que ocupa un lugar en el espacio.
Sistemas materiales
La masa, en física, es la magnitud que cuantifica la cantidad de materia de un cuerpo. La unidad de masa, en el Sistema Internacional de Unidades es el kilogramo (kg). Es una cantidad escalar y no debe confundirse con el peso, que es una fuerza.
Para poder trabajar con las sustancias necesitamos conocer el volumen de los cuerpos que se define como el lugar que ocupa un cuerpo en el espacio, te serán útiles las siguientes Área y volumen de cuerpos
También es necesario conocer las propiedades de los diversos sistemas materiales. Prueba a realizar estas cuestiones
Debes de cargar el programa, apenas ocupa espacio, y luego tienes unas actividades de evaluación. ¡Suerte!
Sistemas materiales
La masa, en física, es la magnitud que cuantifica la cantidad de materia de un cuerpo. La unidad de masa, en el Sistema Internacional de Unidades es el kilogramo (kg). Es una cantidad escalar y no debe confundirse con el peso, que es una fuerza.
Para poder trabajar con las sustancias necesitamos conocer el volumen de los cuerpos que se define como el lugar que ocupa un cuerpo en el espacio, te serán útiles las siguientes Área y volumen de cuerpos
También es necesario conocer las propiedades de los diversos sistemas materiales. Prueba a realizar estas cuestiones
Debes de cargar el programa, apenas ocupa espacio, y luego tienes unas actividades de evaluación. ¡Suerte!
jueves, 24 de septiembre de 2009
LAS REGLAS DEL JUEGO
Os indico en este párrafo las reglas del juego para este curso:
ORDEN 1670/2009, de 16 de abril, por la que se regula para la Comunidad de Madrid la evaluación en las enseñanzas para la obtención del título de graduado en Educación Secundaria Obligatoria por personas adultas y los documentos de aplicación.
Artículo 8
Convocatorias
1. En la modalidad presencial, el alumnado dispondrá de un máximo de cuatro convocatorias para superar cada ámbito de conocimiento de cada nivel, entre las ordinarias y las extraordinarias.
2. Con el fin de no agotar el límite máximo de convocatorias establecidas en el punto 1 de este artículo, los alumnos podrán solicitar la anulación de una o de las dos convocatorias que se celebran en cada curso académico, para todos o para alguno de los ámbitos de conocimiento, siempre que concurra alguna de las siguientes circunstancias:
a) Enfermedad prolongada o accidente del alumno.
b) Desempeñar un puesto de trabajo en un horario incompatible con el que tiene asignado el ámbito para el que solicita la anulación.
c) Obligaciones de tipo personal o familiar apreciadas por el Director del centro que impidan la normal dedicación al estudio.
3. Las razones que se aleguen en la solicitud de anulación siempre deben justificarse documentalmente. En el caso c) el alumno presentará un escrito indicando el tipo de obligación.
4. La solicitud de anulación de la convocatoria se presentará con una antelación mínima de un mes a la fecha de la evaluación final ordinaria del ámbito o ámbitos cuya anulación se solicita. En el caso de las pruebas extraordinarias, el plazo para presentar esta solicitud finalizará el día 30 de junio. El Director del centro resolverá la petición en el plazo máximo de diez días. Una copia de la resolución se adjuntará al expediente académico del alumno.
5. En la modalidad a distancia no existe límite de convocatorias
Capítulo I
Evaluación, promoción y titulación
Artículo 2
Carácter de la evaluación
1. La evaluación del proceso de aprendizaje de los alumnos será continua y diferenciada según los distintos ámbitos en los que se organizan estas enseñanzas.
2. La evaluación continua del alumnado requiere su asistencia regular a las clases y a las actividades programadas para los distintos ámbitos que constituyen el plan de estudios.
3. Los centros establecerán en su reglamento de régimen interior los procedimientos extraordinarios de evaluación para aquellos alumnos que no puedan ser calificados por evaluación continua por presentar un absentismo superior al 25 por 100 del horario lectivo total para cada uno de los ámbitos de cada nivel.
4. Los profesores evaluarán a los alumnos teniendo en cuenta los diferentes elementos del currículo. Los criterios de evaluación
establecidos en el mismo y concretados en las programaciones didácticas serán el referente fundamental para valorar tanto el grado de adquisición de las competencias básicas y de los contenidos como el de la consecución de los objetivos.
5. El proceso de evaluación continua será desarrollado por el equipo docente, integrado por el conjunto de profesores de cada grupo de alumnos, coordinado por el profesor tutor del grupo. La calificación de cada uno de los ámbitos será decidida por el profesor o profesores respectivos. El resto de las decisiones serán adoptadas por consenso del equipo docente. Si ello no fuera posible, se utilizará el criterio de la mayoría absoluta, es decir, más de la mitad de los miembros que integran el equipo docente.
6. Los alumnos podrán realizar una prueba extraordinaria de los ámbitos que no hayan superado en la evaluación final ordinaria. Esta prueba, que se celebrará en los primeros días de septiembre, será elaborada por los departamentos de coordinación didáctica responsables de cada ámbito o quien desarrolle sus funciones en los centros privados, que también establecerán los criterios de calificación.
7. Los profesores evaluarán los aprendizajes de los alumnos, así como los procesos de enseñanza y su propia práctica docente. Los departamentos de coordinación didáctica o quien desarrolle sus funciones en los centros privados, incorporarán en la memoria de fin de curso el análisis de los resultados de dicha evaluación, tanto en lo
que afecta a los alumnos como en lo que afecta a la práctica docente.
8. Las referencias a la evaluación continua no serán de aplicación en las enseñanzas del régimen a distancia.
Artículo 3
Resultados de la evaluación
1. Los resultados de la evaluación en las enseñanzas para la obtención del título de Graduado en Educación Secundaria Obligatoria por personas adultas se expresarán con las siguientes calificaciones cualitativas: Insuficiente (IN), Suficiente (SU), Bien (BI),
Notable (NT), Sobresaliente (SB), considerándose negativa la calificación Insuficiente y positivas todas las demás. Estas expresiones irán acompañadas de una calificación cuantitativa, sin emplear decimales, en una escala de 1 a 10, aplicándose las siguientes correspondencias:
— Insuficiente: 1, 2,3o4.
— Suficiente: 5.
— Bien: 6.
— Notable: 7 u 8.
Sobresaliente: 9 o 10.
— 2. Cada uno de los ámbitos tendrá una única calificación. En el caso de los ámbitos organizados e impartidos de forma modular, ámbito de la comunicación o ámbito científico tecnológico, la calificación será la media aritmética de las calificaciones de cada módulo, redondeada al entero superior más próximo si la cifra de las décimas es igual o superior a 5, o al entero inferior más próximo si
dicha cifra es inferior a 5.
3. Los ámbitos se consideran aprobados cuando tengan calificación positiva y se consideran suspensos cuando la tengan negativa.
Cuando un alumno no se presente a la prueba extraordinaria correspondiente a alguno de los ámbitos calificados con Insuficiente en la evaluación final ordinaria, en los documentos de evaluación se pondrá la expresión “NP”.
4. Cuando alguno de los ámbitos se haya declarado exento por aplicación del Anexo III de la Orden 3888/2008, de 31 de julio, en los documentos de evaluación se hará constar esta circunstancia con la expresión “EX”.
5. Los alumnos deberán superar los ámbitos del nivel I para poder ser calificados de los ámbitos homónimos del nivel II. Cuando un ámbito de nivel II no pueda ser calificado porque el alumno no ha superado el ámbito de nivel I, se computará como pendiente y esta circunstancia se hará constar en los documentos de evaluación.
6. Cuando un ámbito no pueda ser calificado debido a que el alumno se ha acogido a lo establecido en el artículo 13.1 de la mencionada Orden 3888/2008, de 31 de julio, se consignará un guión (-)en los documentos de evaluación.
Saludos a todos
ORDEN 1670/2009, de 16 de abril, por la que se regula para la Comunidad de Madrid la evaluación en las enseñanzas para la obtención del título de graduado en Educación Secundaria Obligatoria por personas adultas y los documentos de aplicación.
Artículo 8
Convocatorias
1. En la modalidad presencial, el alumnado dispondrá de un máximo de cuatro convocatorias para superar cada ámbito de conocimiento de cada nivel, entre las ordinarias y las extraordinarias.
2. Con el fin de no agotar el límite máximo de convocatorias establecidas en el punto 1 de este artículo, los alumnos podrán solicitar la anulación de una o de las dos convocatorias que se celebran en cada curso académico, para todos o para alguno de los ámbitos de conocimiento, siempre que concurra alguna de las siguientes circunstancias:
a) Enfermedad prolongada o accidente del alumno.
b) Desempeñar un puesto de trabajo en un horario incompatible con el que tiene asignado el ámbito para el que solicita la anulación.
c) Obligaciones de tipo personal o familiar apreciadas por el Director del centro que impidan la normal dedicación al estudio.
3. Las razones que se aleguen en la solicitud de anulación siempre deben justificarse documentalmente. En el caso c) el alumno presentará un escrito indicando el tipo de obligación.
4. La solicitud de anulación de la convocatoria se presentará con una antelación mínima de un mes a la fecha de la evaluación final ordinaria del ámbito o ámbitos cuya anulación se solicita. En el caso de las pruebas extraordinarias, el plazo para presentar esta solicitud finalizará el día 30 de junio. El Director del centro resolverá la petición en el plazo máximo de diez días. Una copia de la resolución se adjuntará al expediente académico del alumno.
5. En la modalidad a distancia no existe límite de convocatorias
Capítulo I
Evaluación, promoción y titulación
Artículo 2
Carácter de la evaluación
1. La evaluación del proceso de aprendizaje de los alumnos será continua y diferenciada según los distintos ámbitos en los que se organizan estas enseñanzas.
2. La evaluación continua del alumnado requiere su asistencia regular a las clases y a las actividades programadas para los distintos ámbitos que constituyen el plan de estudios.
3. Los centros establecerán en su reglamento de régimen interior los procedimientos extraordinarios de evaluación para aquellos alumnos que no puedan ser calificados por evaluación continua por presentar un absentismo superior al 25 por 100 del horario lectivo total para cada uno de los ámbitos de cada nivel.
4. Los profesores evaluarán a los alumnos teniendo en cuenta los diferentes elementos del currículo. Los criterios de evaluación
establecidos en el mismo y concretados en las programaciones didácticas serán el referente fundamental para valorar tanto el grado de adquisición de las competencias básicas y de los contenidos como el de la consecución de los objetivos.
5. El proceso de evaluación continua será desarrollado por el equipo docente, integrado por el conjunto de profesores de cada grupo de alumnos, coordinado por el profesor tutor del grupo. La calificación de cada uno de los ámbitos será decidida por el profesor o profesores respectivos. El resto de las decisiones serán adoptadas por consenso del equipo docente. Si ello no fuera posible, se utilizará el criterio de la mayoría absoluta, es decir, más de la mitad de los miembros que integran el equipo docente.
6. Los alumnos podrán realizar una prueba extraordinaria de los ámbitos que no hayan superado en la evaluación final ordinaria. Esta prueba, que se celebrará en los primeros días de septiembre, será elaborada por los departamentos de coordinación didáctica responsables de cada ámbito o quien desarrolle sus funciones en los centros privados, que también establecerán los criterios de calificación.
7. Los profesores evaluarán los aprendizajes de los alumnos, así como los procesos de enseñanza y su propia práctica docente. Los departamentos de coordinación didáctica o quien desarrolle sus funciones en los centros privados, incorporarán en la memoria de fin de curso el análisis de los resultados de dicha evaluación, tanto en lo
que afecta a los alumnos como en lo que afecta a la práctica docente.
8. Las referencias a la evaluación continua no serán de aplicación en las enseñanzas del régimen a distancia.
Artículo 3
Resultados de la evaluación
1. Los resultados de la evaluación en las enseñanzas para la obtención del título de Graduado en Educación Secundaria Obligatoria por personas adultas se expresarán con las siguientes calificaciones cualitativas: Insuficiente (IN), Suficiente (SU), Bien (BI),
Notable (NT), Sobresaliente (SB), considerándose negativa la calificación Insuficiente y positivas todas las demás. Estas expresiones irán acompañadas de una calificación cuantitativa, sin emplear decimales, en una escala de 1 a 10, aplicándose las siguientes correspondencias:
— Insuficiente: 1, 2,3o4.
— Suficiente: 5.
— Bien: 6.
— Notable: 7 u 8.
Sobresaliente: 9 o 10.
— 2. Cada uno de los ámbitos tendrá una única calificación. En el caso de los ámbitos organizados e impartidos de forma modular, ámbito de la comunicación o ámbito científico tecnológico, la calificación será la media aritmética de las calificaciones de cada módulo, redondeada al entero superior más próximo si la cifra de las décimas es igual o superior a 5, o al entero inferior más próximo si
dicha cifra es inferior a 5.
3. Los ámbitos se consideran aprobados cuando tengan calificación positiva y se consideran suspensos cuando la tengan negativa.
Cuando un alumno no se presente a la prueba extraordinaria correspondiente a alguno de los ámbitos calificados con Insuficiente en la evaluación final ordinaria, en los documentos de evaluación se pondrá la expresión “NP”.
4. Cuando alguno de los ámbitos se haya declarado exento por aplicación del Anexo III de la Orden 3888/2008, de 31 de julio, en los documentos de evaluación se hará constar esta circunstancia con la expresión “EX”.
5. Los alumnos deberán superar los ámbitos del nivel I para poder ser calificados de los ámbitos homónimos del nivel II. Cuando un ámbito de nivel II no pueda ser calificado porque el alumno no ha superado el ámbito de nivel I, se computará como pendiente y esta circunstancia se hará constar en los documentos de evaluación.
6. Cuando un ámbito no pueda ser calificado debido a que el alumno se ha acogido a lo establecido en el artículo 13.1 de la mencionada Orden 3888/2008, de 31 de julio, se consignará un guión (-)en los documentos de evaluación.
Saludos a todos
Se acabó lo que se daba
Pués sí,señores, se acabó lo que se daba.
Se acabaron las vacaciones para ustedes. Volvemos a trabajar con el yogur de fabada y otras nuevas recetas, que se irán incorporando en breve, durante este curso. Espero que sigan pasando por este lugar y hagán sus comentarios. Dentro de muy poco tiempo,estaremos de nuevo en marcha.
Saludos
Se acabaron las vacaciones para ustedes. Volvemos a trabajar con el yogur de fabada y otras nuevas recetas, que se irán incorporando en breve, durante este curso. Espero que sigan pasando por este lugar y hagán sus comentarios. Dentro de muy poco tiempo,estaremos de nuevo en marcha.
Saludos
lunes, 22 de junio de 2009
CERRADO POR VACACIONES
Pues si, al igual que se veia, hace algún tiempo en las tiendas de Madrid, cierro por vacaciones. Aunque del blog para adentro seguiré trabajando en los proyectos de mis amigos Carlos y Jose Antonio, así como en otros tres míos. Con este panorama de trabajo, ya no sé si cierro o abro.
espeo que sigais pasando por aquí. por cierto Exclusiva :la receta del Yogur de Fabada, está pendiente de algunos retoques.
Besos y abrazos según corresponda
espeo que sigais pasando por aquí. por cierto Exclusiva :la receta del Yogur de Fabada, está pendiente de algunos retoques.
Besos y abrazos según corresponda
domingo, 7 de junio de 2009
NUMEROS GORDOS
6.000 millones de Euros equivalen a un BILLÓN de las antiguas pesetas.
5.340.000 Euros son las retribuciones recibidas durante 2008 por D. Francisco González, Presidente del BBVA. Esta cantidad equivalen a casi 445 años de salario de un milEurista.
17.590 millones de Euros son los beneficios obtenidos por los 'cinco grandes de la banca española'. Esa cantidad equivale a 2,93 Billones de la antiguas pesetas. También a 1.465.833 de años de trabajo de un milEurista.
2.500 millones de personas SOBREVIVEN con menos de 1,50 Euros al día.
viernes, 29 de mayo de 2009
LA CURIOSIDAD DEL MES
EN ESTA ÉPOCA DE EXÁMENES ES BUENO RECORDAR LOS
PROCESOS EN LA CAFETERA ITALIANA (la de casa de toda la vida)
El café molido se sitúa en el receptáculo del embudo mientras que en el cuerpo inferior se deposita agua. Se calienta el agua y entonces empieza a formarse vapor que ejerce presión sobre el resto del agua y la empuja a través del tubo inferior; el agua a presión atraviesa la masa del café produciéndose entonces el proceso de extracción de las sustancias solubles.
Aunque algunos autores piensan que la extracción se hace por una mezcla de agua y vapor, la realidad observada por nosotros es que la cantidad de vapor que circula por el sistema, al menos en las primeras fases de la extracción, es ínfima, debiéndose hablar pues de una extracción por líquido a presión, no muy superior a la atmosférica. Sólo al final cuando ya se ha agotado el agua pasa algo de vapor, son los clásicos “tosidos” finales de la cafetera. Es decir, el vapor sirve para “empujar el agua”, no para extraer las sustancias.
Normalmente las cafeteras, como medida de seguridad, llevan una válvula en su cuerpo inferior.
Se trata ahora de seguir con un poco de detenimiento lo que ocurre en la cafetera.
La bebida que conocemos como café es agua que contiene, por una parte, una serie de sustancias solubles procedentes del café, tales como la cafeína, los restos de azúcares, ácidos y otras sustancias polares, y por otra, sustancias no solubles que se emulsionan en el agua.
El proceso por el cual estas sustancias se extraen del café molido y pasan al agua puede englobarse, como todo proceso de este tipo, en una difusión de las sustancias en el propio grano, y el paso a través de la resistencia correspondiente a la fase acuosa.
El mecanismo de difusión en líquidos y sólido – líquido, a diferencia del de gases, no esta suficientemente establecido. Sin embargo, en línea generales, se puede afirmar que el paso se debe a una fuerza impulsora, un gradiente, en este caso de concentración y, posiblemente, también de presión1 (McCabe,1981). En este sentido, las cafeteras de émbolo o italianas mejoran las cualidades del café. De todos modos, vista la variación de temperatura no parece que sea oportuno en la cafetera italiana hablar de una presión importante.
Al no conseguirse las presiones de las máquinas express el resultado no es un “auténtico café express”, pero se le asemeja bastante.
El café express es una sistema coloidal polifásico en el que hay burbujas de gas, restos sólidos, aceites que a su veces llevan disueltos aromas liposolubles en forma de micelas de menos de 5m de diámetro medio, por esta razón la viscosidad del liquido aumenta ya adquiere “más cuerpo”, de modo que al beberlo, literalmente recubre la lengua con una fina capa y continua liberando volátiles, la cavidad bucal está a unos 37º, lo que favorece esta liberación, por lo que el sabor del café permanece largo rato después de su ingesta. (En algunos países, se acostumbra a beber un vaso de agua después del café suponemos que para evitar la liberación de sabores indeseados, algunos tal vez inducidos por los enzimas de la saliva)
En la infusión, como ya se ha dicho en otras partes de este trabajo, hay abundantes productos volátiles a los que se debe buena parte del aroma del café y que se pierden con el tiempo, de ahí las rectas populares que previenen contra el café recalentado o hervido, incluso en el momento de la preparación.
Mi agradecimiento a mi amigo J.A.M. PONS
PROCESOS EN LA CAFETERA ITALIANA (la de casa de toda la vida)
El café molido se sitúa en el receptáculo del embudo mientras que en el cuerpo inferior se deposita agua. Se calienta el agua y entonces empieza a formarse vapor que ejerce presión sobre el resto del agua y la empuja a través del tubo inferior; el agua a presión atraviesa la masa del café produciéndose entonces el proceso de extracción de las sustancias solubles.
Aunque algunos autores piensan que la extracción se hace por una mezcla de agua y vapor, la realidad observada por nosotros es que la cantidad de vapor que circula por el sistema, al menos en las primeras fases de la extracción, es ínfima, debiéndose hablar pues de una extracción por líquido a presión, no muy superior a la atmosférica. Sólo al final cuando ya se ha agotado el agua pasa algo de vapor, son los clásicos “tosidos” finales de la cafetera. Es decir, el vapor sirve para “empujar el agua”, no para extraer las sustancias.
Normalmente las cafeteras, como medida de seguridad, llevan una válvula en su cuerpo inferior.
Se trata ahora de seguir con un poco de detenimiento lo que ocurre en la cafetera.
La bebida que conocemos como café es agua que contiene, por una parte, una serie de sustancias solubles procedentes del café, tales como la cafeína, los restos de azúcares, ácidos y otras sustancias polares, y por otra, sustancias no solubles que se emulsionan en el agua.
El proceso por el cual estas sustancias se extraen del café molido y pasan al agua puede englobarse, como todo proceso de este tipo, en una difusión de las sustancias en el propio grano, y el paso a través de la resistencia correspondiente a la fase acuosa.
El mecanismo de difusión en líquidos y sólido – líquido, a diferencia del de gases, no esta suficientemente establecido. Sin embargo, en línea generales, se puede afirmar que el paso se debe a una fuerza impulsora, un gradiente, en este caso de concentración y, posiblemente, también de presión1 (McCabe,1981). En este sentido, las cafeteras de émbolo o italianas mejoran las cualidades del café. De todos modos, vista la variación de temperatura no parece que sea oportuno en la cafetera italiana hablar de una presión importante.
Al no conseguirse las presiones de las máquinas express el resultado no es un “auténtico café express”, pero se le asemeja bastante.
El café express es una sistema coloidal polifásico en el que hay burbujas de gas, restos sólidos, aceites que a su veces llevan disueltos aromas liposolubles en forma de micelas de menos de 5m de diámetro medio, por esta razón la viscosidad del liquido aumenta ya adquiere “más cuerpo”, de modo que al beberlo, literalmente recubre la lengua con una fina capa y continua liberando volátiles, la cavidad bucal está a unos 37º, lo que favorece esta liberación, por lo que el sabor del café permanece largo rato después de su ingesta. (En algunos países, se acostumbra a beber un vaso de agua después del café suponemos que para evitar la liberación de sabores indeseados, algunos tal vez inducidos por los enzimas de la saliva)
En la infusión, como ya se ha dicho en otras partes de este trabajo, hay abundantes productos volátiles a los que se debe buena parte del aroma del café y que se pierden con el tiempo, de ahí las rectas populares que previenen contra el café recalentado o hervido, incluso en el momento de la preparación.
Mi agradecimiento a mi amigo J.A.M. PONS
jueves, 21 de mayo de 2009
ENERGIA, TRABAJO Y POTENCIA
El concepto de energía es uno de los más importantes de la ciencia. Todo cambio o proceso en la naturaleza se relaciona con la energía. Y así como existe una variedad de fenómenos diferentes como calentar agua, encender una lámpara, quemar un papel, golpear un clavo con el martillo o pulsar la cuerda de una guitarra, aparecen diferentes tipos de energía involucrados: térmica, eléctrica, lumínica, química, de movimiento, etc.
Es difícil decir qué es la energía; actualmente la ciencia no dispone de una definición precisa del término (como expresó en cierta oportunidad el premio Nobel de física Richard Feynman “Es importante constatar que en la física de hoy, no sabemos lo que es la energía.”).
Pero el hecho de no poder definirla no nos impide que la utilicemos, la reconozcamos y sepamos cosas de ella. Después de todo, que nos resulte muy difícil definir el color rojo, no nos limita para que reconozcamos la luz roja del semáforo, pintemos de rojo un banquito de la cocina o llamemos a un equipo de fútbol “los rojos del Osasuna ”. Pero, más allá de la simple analogía, parece ser que cuánto más fundamental es un concepto más complicado es definirlo: energía, masa y tiempo están en esta categoría.
Todo parece indicar que la energía tiene dos características básicas: por un lado no se crea ni se destruye y, en segundo lugar, puede cambiar de un tipo de energía a otro. (para que estas definiciones fuesen rigurosamente válidas deberíamos incluir a la masa como otra manifestación de la energía, pero para nuestros objetivos es suficiente considerarla de esa manera).
De acuerdo con lo dicho cuando un tipo de energía “desaparece” o “se gasta” alguna otra forma aparece. A modo de ejemplos:
• La energía eléctrica suministrada por las pilas se transforman en luz y calor al encender una linterna
• La energía de movimiento que ponemos en juego al frotar nuestras manos se traduce en calor
• La energía acumulada al tensar un arco se transformará, al liberarlo, en energía de movimiento de la flecha.
En Física nos detendremos a analizar tres de esos tipos de energía: la de movimiento (cinética), las que tienen que ver con fuerzas (potenciales) y la que está relacionada con el calor (térmica).
La Energía Cinética es la que posee un cuerpo que se está moviendo. La energía de un cuerpo en movimiento depende de dos características fundamentales: su masa y la velocidad.
Como siempre, es posible deducir una expresión matemática que indique la relación entre las magnitudes y nos sirva para calcular la energía cinética de un objeto. Si bien el desarrollo no es complejo nos limitaremos a contar el final de la historia y diremos que EC = ½ m.v2 (un medio de la masa por el cuadrado de la velocidad). Esta ecuación nos muestra que la energía de un cuerpo en movimiento es proporcional a su masa, es decir, si un cuerpo tiene el doble de masa que otro, y ambos se mueven con la misma velocidad, el primero tiene el doble de energía cinética. Por otro lado, la energía es directamente proporcional al cuadrado de la velocidad. Esto significa que si dos objetos tienen la misma masa, y uno se desplaza con el doble de velocidad que el otro, el que va más rápido posee cuatro veces más energía de movimiento.
Supongamos sostener, quieto, un objeto a cierta altura del suelo. Podría ser una moneda, un florero, sus anteojos o cualquier otro objeto, para el caso da lo mismo (eso sí, si va a hacer el ensayo experimental, elija el primero; aprender aprenderá igual y se ahorrará un dolor de cabeza). Este objeto, quieto donde está, no posee energía cinética ya que, si bien tiene masa, su velocidad es cero. ¿Qué ocurre si soltamos el objeto? Debido a la fuerza de atracción gravitatoria el cuerpo comenzará a caer aumentando progresivamente su velocidad. Despreciando la resistencia del aire podemos admitir que cae en caída libre. Al final del recorrido, y justo antes de chocar, el objeto habrá adquirido su máxima velocidad producto de haber estado acelerando durante todo el recorrido. Salvo en el instante inicial (cuando su velocidad era cero), el objeto tendrá una energía cinética que irá en aumento. Pero ¿de dónde sale esta energía?. Tal como expresamos más arriba la energía no puede crearse de la nada. Si "aparece" energía cinética es porque algún otro tipo de energía está "desapareciendo". Dicho de otra manera: se produjo una transformación de energía. Esta otra energía, estaba almacenada o acumulada en el cuerpo cuando se encontraba quieto a cierta distancia del suelo y fue, a lo largo del recorrido, transformándose en energía cinética. A esta energía que el objeto tiene almacenada la llamamos Energía Potencial Gravitatoria o Gravitacional. Se la suele llamar energía de posición porque depende del lugar donde se encuentra el objeto.
Las energías potenciales están asociadas a fuerzas y, a diferencia de la energía cinética que es algo perteneciente al cuerpo, las energías potenciales involucran un sistema (recordemos que las fuerzas son resultados de interacciones). La energía potencial gravitacional tiene que ver con las fuerzas gravitatorias, pero existe energía potencial elástica, eléctrica, etc., dependiendo del tipo de interacción involucrada.
Presentamos aquí la ecuación que permite calcular la energía potencial gravitacional de un cuerpo y estimar la relación entre las magnitudes: Ep = m. g. h (masa por aceleración de la gravedad por altura). Vemos que existe una proporcionalidad directa entre la energía y las tres magnitudes que la definen. Esto significa que, por ejemplo:
• Un piano tiene más energía potencial gravitatoria que un ratón si ambos se encuentran a la misma altura de la superficie terrestre
• Una misma maceta tiene más energía potencial gravitacional si se encuentra en el balcón del piso 12 que en el del piso 5
• La energía potencial de un martillo es mayor cuando es sostenido por un astronauta, a una misma altura, en la Tierra que en la Luna ( donde g es seis veces menor)
Sólo un par de cosas más acerca de la energía.
• Se define la Energía Mecánica como la suma de las energías cinética y potencial de un cuerpo. En símbolos EM = Ec + Ep.
• La unidad en que se expresa la energía en el sistema internacional es el Joule. Es una unidad derivada y compuesta Joule = kg.m2/s2 (kilogramo por metro cuadrado sobre segundo cuadrado)
Hasta aquí hemos analizado esta cuestión de la energía mecánica: definiciones, características, ecuaciones y unidades. Queda para otro encuentro discutir un aspecto de suma importancia para la física que es la ley de conservación de la energía.
Por ahora es bastante ... vaya, descanse, tome algo y... reponga energía.
(Tomado del Blog de Pablo-Físicaadultos),
ir a Energía Mecánica (II)
Es difícil decir qué es la energía; actualmente la ciencia no dispone de una definición precisa del término (como expresó en cierta oportunidad el premio Nobel de física Richard Feynman “Es importante constatar que en la física de hoy, no sabemos lo que es la energía.”).
Pero el hecho de no poder definirla no nos impide que la utilicemos, la reconozcamos y sepamos cosas de ella. Después de todo, que nos resulte muy difícil definir el color rojo, no nos limita para que reconozcamos la luz roja del semáforo, pintemos de rojo un banquito de la cocina o llamemos a un equipo de fútbol “los rojos del Osasuna ”. Pero, más allá de la simple analogía, parece ser que cuánto más fundamental es un concepto más complicado es definirlo: energía, masa y tiempo están en esta categoría.
Todo parece indicar que la energía tiene dos características básicas: por un lado no se crea ni se destruye y, en segundo lugar, puede cambiar de un tipo de energía a otro. (para que estas definiciones fuesen rigurosamente válidas deberíamos incluir a la masa como otra manifestación de la energía, pero para nuestros objetivos es suficiente considerarla de esa manera).
De acuerdo con lo dicho cuando un tipo de energía “desaparece” o “se gasta” alguna otra forma aparece. A modo de ejemplos:
• La energía eléctrica suministrada por las pilas se transforman en luz y calor al encender una linterna
• La energía de movimiento que ponemos en juego al frotar nuestras manos se traduce en calor
• La energía acumulada al tensar un arco se transformará, al liberarlo, en energía de movimiento de la flecha.
En Física nos detendremos a analizar tres de esos tipos de energía: la de movimiento (cinética), las que tienen que ver con fuerzas (potenciales) y la que está relacionada con el calor (térmica).
La Energía Cinética es la que posee un cuerpo que se está moviendo. La energía de un cuerpo en movimiento depende de dos características fundamentales: su masa y la velocidad.
Como siempre, es posible deducir una expresión matemática que indique la relación entre las magnitudes y nos sirva para calcular la energía cinética de un objeto. Si bien el desarrollo no es complejo nos limitaremos a contar el final de la historia y diremos que EC = ½ m.v2 (un medio de la masa por el cuadrado de la velocidad). Esta ecuación nos muestra que la energía de un cuerpo en movimiento es proporcional a su masa, es decir, si un cuerpo tiene el doble de masa que otro, y ambos se mueven con la misma velocidad, el primero tiene el doble de energía cinética. Por otro lado, la energía es directamente proporcional al cuadrado de la velocidad. Esto significa que si dos objetos tienen la misma masa, y uno se desplaza con el doble de velocidad que el otro, el que va más rápido posee cuatro veces más energía de movimiento.
Supongamos sostener, quieto, un objeto a cierta altura del suelo. Podría ser una moneda, un florero, sus anteojos o cualquier otro objeto, para el caso da lo mismo (eso sí, si va a hacer el ensayo experimental, elija el primero; aprender aprenderá igual y se ahorrará un dolor de cabeza). Este objeto, quieto donde está, no posee energía cinética ya que, si bien tiene masa, su velocidad es cero. ¿Qué ocurre si soltamos el objeto? Debido a la fuerza de atracción gravitatoria el cuerpo comenzará a caer aumentando progresivamente su velocidad. Despreciando la resistencia del aire podemos admitir que cae en caída libre. Al final del recorrido, y justo antes de chocar, el objeto habrá adquirido su máxima velocidad producto de haber estado acelerando durante todo el recorrido. Salvo en el instante inicial (cuando su velocidad era cero), el objeto tendrá una energía cinética que irá en aumento. Pero ¿de dónde sale esta energía?. Tal como expresamos más arriba la energía no puede crearse de la nada. Si "aparece" energía cinética es porque algún otro tipo de energía está "desapareciendo". Dicho de otra manera: se produjo una transformación de energía. Esta otra energía, estaba almacenada o acumulada en el cuerpo cuando se encontraba quieto a cierta distancia del suelo y fue, a lo largo del recorrido, transformándose en energía cinética. A esta energía que el objeto tiene almacenada la llamamos Energía Potencial Gravitatoria o Gravitacional. Se la suele llamar energía de posición porque depende del lugar donde se encuentra el objeto.
Las energías potenciales están asociadas a fuerzas y, a diferencia de la energía cinética que es algo perteneciente al cuerpo, las energías potenciales involucran un sistema (recordemos que las fuerzas son resultados de interacciones). La energía potencial gravitacional tiene que ver con las fuerzas gravitatorias, pero existe energía potencial elástica, eléctrica, etc., dependiendo del tipo de interacción involucrada.
Presentamos aquí la ecuación que permite calcular la energía potencial gravitacional de un cuerpo y estimar la relación entre las magnitudes: Ep = m. g. h (masa por aceleración de la gravedad por altura). Vemos que existe una proporcionalidad directa entre la energía y las tres magnitudes que la definen. Esto significa que, por ejemplo:
• Un piano tiene más energía potencial gravitatoria que un ratón si ambos se encuentran a la misma altura de la superficie terrestre
• Una misma maceta tiene más energía potencial gravitacional si se encuentra en el balcón del piso 12 que en el del piso 5
• La energía potencial de un martillo es mayor cuando es sostenido por un astronauta, a una misma altura, en la Tierra que en la Luna ( donde g es seis veces menor)
Sólo un par de cosas más acerca de la energía.
• Se define la Energía Mecánica como la suma de las energías cinética y potencial de un cuerpo. En símbolos EM = Ec + Ep.
• La unidad en que se expresa la energía en el sistema internacional es el Joule. Es una unidad derivada y compuesta Joule = kg.m2/s2 (kilogramo por metro cuadrado sobre segundo cuadrado)
Hasta aquí hemos analizado esta cuestión de la energía mecánica: definiciones, características, ecuaciones y unidades. Queda para otro encuentro discutir un aspecto de suma importancia para la física que es la ley de conservación de la energía.
Por ahora es bastante ... vaya, descanse, tome algo y... reponga energía.
(Tomado del Blog de Pablo-Físicaadultos),
ir a Energía Mecánica (II)
jueves, 23 de abril de 2009
Ejercicios de Presión
1. Calcular la presión que ejerce un cuerpo de 120 kg que está apoyado sobre una superficie de 0,8 m2.
2. Si el mismo cuerpo del problema anterior se apoya sobre una superficie de 1,2 m 2,¿qué presión ejercerá?, compare y deduzca las conclusiones.
3. Los radios de los émbolos de una prensa hidráulica son de 10 cm y 50 cm respectivamente. ¿Qué fuerza ejercerá el émbolo mayor si sobre el menor actúa una de 30 N?.
4. Un cubo de aluminio (δ = 2,7 g/cm ³) de 4 cm de lado se coloca en agua de mar (δ = 1,025g/cm ³), ¿flota o se hunde?.
5. Si el cubo del problema anterior se coloca en mercurio (δ = 13,6 g/cm ³), ¿flota o se hunde?.
6. Un recipiente cilíndrico contiene aceite (ρ = 0,92 g/cm ³) hasta 30 cm de altura. Calcular el peso del aceite y la presión que ejerce sobre el fondo, sabiendo que el radio del cilindro es de 10 cm.
7. Un prisma de bronce de 2 m de largo por 0,85m de alto por 2 cm de ancho se apoya sobre la base de 2 m por 0.85 m, ¿qué presión ejerce, si la densidad del bronce es de 8,8 g/cm ³?.
8. ¿Cuál será el peso de un cuerpo que apoyado sobre una base de 75 cm ² ejerce una presión de 200 bares?.
9. Las secciones de los émbolos de una prensa hidráulica son de 8 cm ² y de 20 cm ² respectivamente. Si sobre el primero se aplica una fuerza de 70 N, ¿cuál será la fuerza obtenida por el otro émbolo?.
10. Sobre el émbolo de 12 cm ² de un prensa hidráulica se aplica una fuerza de 40 N, en el otro se obtiene una fuerza de 150 N, ¿qué sección tiene éste émbolo?.
11. Un cuerpo ejerce una presión de 35 bar, si pesa 200 N, ¿cuánto vale la superficie de apoyo?.
12. Si un cubo de hierro de 30 cm de lado está apoyado sobre una cara, ¿qué presión ejerce? (δ = 7,8 g/cm ³).
13. El radio del émbolo menor de una prensa es de 4 cm, si sobre él se aplica una fuerza de 60 N se obtiene en el otro émbolo una de 300 N, ¿cuál es el radio de éste émbolo?.
14. Sobre el émbolo menor de una prensa se aplica una fuerza de 50 N, si en el otro se obtiene una de 1000 N, ¿cuál es la relación entre los radios de los émbolos?.
2. Si el mismo cuerpo del problema anterior se apoya sobre una superficie de 1,2 m 2,¿qué presión ejercerá?, compare y deduzca las conclusiones.
3. Los radios de los émbolos de una prensa hidráulica son de 10 cm y 50 cm respectivamente. ¿Qué fuerza ejercerá el émbolo mayor si sobre el menor actúa una de 30 N?.
4. Un cubo de aluminio (δ = 2,7 g/cm ³) de 4 cm de lado se coloca en agua de mar (δ = 1,025g/cm ³), ¿flota o se hunde?.
5. Si el cubo del problema anterior se coloca en mercurio (δ = 13,6 g/cm ³), ¿flota o se hunde?.
6. Un recipiente cilíndrico contiene aceite (ρ = 0,92 g/cm ³) hasta 30 cm de altura. Calcular el peso del aceite y la presión que ejerce sobre el fondo, sabiendo que el radio del cilindro es de 10 cm.
7. Un prisma de bronce de 2 m de largo por 0,85m de alto por 2 cm de ancho se apoya sobre la base de 2 m por 0.85 m, ¿qué presión ejerce, si la densidad del bronce es de 8,8 g/cm ³?.
8. ¿Cuál será el peso de un cuerpo que apoyado sobre una base de 75 cm ² ejerce una presión de 200 bares?.
9. Las secciones de los émbolos de una prensa hidráulica son de 8 cm ² y de 20 cm ² respectivamente. Si sobre el primero se aplica una fuerza de 70 N, ¿cuál será la fuerza obtenida por el otro émbolo?.
10. Sobre el émbolo de 12 cm ² de un prensa hidráulica se aplica una fuerza de 40 N, en el otro se obtiene una fuerza de 150 N, ¿qué sección tiene éste émbolo?.
11. Un cuerpo ejerce una presión de 35 bar, si pesa 200 N, ¿cuánto vale la superficie de apoyo?.
12. Si un cubo de hierro de 30 cm de lado está apoyado sobre una cara, ¿qué presión ejerce? (δ = 7,8 g/cm ³).
13. El radio del émbolo menor de una prensa es de 4 cm, si sobre él se aplica una fuerza de 60 N se obtiene en el otro émbolo una de 300 N, ¿cuál es el radio de éste émbolo?.
14. Sobre el émbolo menor de una prensa se aplica una fuerza de 50 N, si en el otro se obtiene una de 1000 N, ¿cuál es la relación entre los radios de los émbolos?.
Principio de Arquímedes
EQUILIBRIO DE SOLIDOS
Empuje hidrostático: principio de Arquímedes
Los cuerpos sólidos sumergidos en un líquido experimentan un empuje hacia arriba. Este fenómeno, que es el fundamento de la flotación de los barcos, era conocido desde la más remota antigüedad, pero fue el griego Arquímedes (287-212 a. de C.) quien indicó cuál es la magnitud de dicho empuje. De acuerdo con el principio que lleva su nombre, todo cuerpo sumergido total o parcialmente en un líquido experimenta un empuje vertical y hacia arriba igual al peso del volumen de líquido desalojado.
Aun cuando para llegar a esta conclusión Arquímedes se apoyó en la medida y experimentación, su famoso principio puede ser obtenido como una consecuencia de la ecuación fundamental de la hidrostática. Considérese un cuerpo en forma de paralelepípedo, las longitudes de cuyas aristas valen a, b y c metros, siendo c la correspondiente a la arista vertical. Dado que las fuerzas laterales se compensan mutuamente, sólo se considerarán las fuerzas sobre las caras horizontales. La fuerza F1 sobre la cara superior estará dirigida hacia abajo y de acuerdo con la ecuación fundamental de la hidrostática su magnitud se podrá escribir como
F1 = p1.S1 = (p0 + δ.g.h1).S1
siendo S1 la superficie de la cara superior y h1 su altura respecto de la superficie libre del líquido. La fuerza F2 sobre la cara inferior estará dirigida hacia arriba y, como en el caso anterior, su magnitud será dada por:
F2 = p2.S2 = (p0 + δ.g.h2).S2
La resultante de ambas representará la fuerza de empuje hidrostático E.
E = F2 - F1 = (p0 + δ.g.h2).S2 - (p0 + δ.g.h1).S1
pero, dado que S1 = S2 = S y h2 = h1 + c, resulta:
E = δ.g.c.S = δ.g.V = m.g
que es precisamente el valor del empuje predicho por Arquímedes en su principio, ya que V = c.S es el volumen del cuerpo, ρ la densidad del líquido ,m = ρ .V la masa del líquido desalojado y finalmente m.g es el peso de un volumen de líquido igual al del cuerpo sumergido.
Equilibrio de los cuerpos sumergidos
De acuerdo con el principio de Arquímedes, para que un cuerpo sumergido en un líquido esté en equilibrio, la fuerza de empuje E y el peso P han de ser iguales en magnitudes y, además, han de aplicarse en el mismo punto. En tal caso la fuerza resultante R es cero y también lo es el momento M, con lo cual se dan las dos condiciones de equilibrio. La condición E = P equivale de hecho a que las densidades del cuerpo y del líquido sean iguales. En tal caso el equilibrio del cuerpo sumergido es indiferente.
Si el cuerpo no es homogéneo, el centro de gravedad no coincide con el centro geométrico, que es el punto en donde puede considerarse aplicada la fuerza de empuje. Ello significa que las fuerzas E y P forman un par que hará girar el cuerpo hasta que ambas estén alineadas.
Equilibrio de los cuerpos flotantes
Si un cuerpo sumergido sale a flote es porque el empuje predomina sobre el peso (E >P). En el equilibrio ambas fuerzas aplicadas sobre puntos diferentes estarán alineadas; tal es el caso de las embarcaciones en aguas tranquilas, por ejemplo. Si por efecto de una fuerza lateral, como la producida por un golpe de mar, el eje vertical del navío se inclinara hacia un lado, aparecerá un par de fuerzas que harán oscilar el barco de un lado a otro. Cuanto mayor sea el momento M del par, mayor será la estabilidad del navío, es decir, la capacidad para recuperar la verticalidad. Ello se consigue diseñando convenientemente el casco y repartiendo la carga de modo que rebaje la posición del centro de gravedad, con lo que se consigue aumentar el brazo del par.
"Fisicanet dixit"
Empuje hidrostático: principio de Arquímedes
Los cuerpos sólidos sumergidos en un líquido experimentan un empuje hacia arriba. Este fenómeno, que es el fundamento de la flotación de los barcos, era conocido desde la más remota antigüedad, pero fue el griego Arquímedes (287-212 a. de C.) quien indicó cuál es la magnitud de dicho empuje. De acuerdo con el principio que lleva su nombre, todo cuerpo sumergido total o parcialmente en un líquido experimenta un empuje vertical y hacia arriba igual al peso del volumen de líquido desalojado.
Aun cuando para llegar a esta conclusión Arquímedes se apoyó en la medida y experimentación, su famoso principio puede ser obtenido como una consecuencia de la ecuación fundamental de la hidrostática. Considérese un cuerpo en forma de paralelepípedo, las longitudes de cuyas aristas valen a, b y c metros, siendo c la correspondiente a la arista vertical. Dado que las fuerzas laterales se compensan mutuamente, sólo se considerarán las fuerzas sobre las caras horizontales. La fuerza F1 sobre la cara superior estará dirigida hacia abajo y de acuerdo con la ecuación fundamental de la hidrostática su magnitud se podrá escribir como
F1 = p1.S1 = (p0 + δ.g.h1).S1
siendo S1 la superficie de la cara superior y h1 su altura respecto de la superficie libre del líquido. La fuerza F2 sobre la cara inferior estará dirigida hacia arriba y, como en el caso anterior, su magnitud será dada por:
F2 = p2.S2 = (p0 + δ.g.h2).S2
La resultante de ambas representará la fuerza de empuje hidrostático E.
E = F2 - F1 = (p0 + δ.g.h2).S2 - (p0 + δ.g.h1).S1
pero, dado que S1 = S2 = S y h2 = h1 + c, resulta:
E = δ.g.c.S = δ.g.V = m.g
que es precisamente el valor del empuje predicho por Arquímedes en su principio, ya que V = c.S es el volumen del cuerpo, ρ la densidad del líquido ,m = ρ .V la masa del líquido desalojado y finalmente m.g es el peso de un volumen de líquido igual al del cuerpo sumergido.
Equilibrio de los cuerpos sumergidos
De acuerdo con el principio de Arquímedes, para que un cuerpo sumergido en un líquido esté en equilibrio, la fuerza de empuje E y el peso P han de ser iguales en magnitudes y, además, han de aplicarse en el mismo punto. En tal caso la fuerza resultante R es cero y también lo es el momento M, con lo cual se dan las dos condiciones de equilibrio. La condición E = P equivale de hecho a que las densidades del cuerpo y del líquido sean iguales. En tal caso el equilibrio del cuerpo sumergido es indiferente.
Si el cuerpo no es homogéneo, el centro de gravedad no coincide con el centro geométrico, que es el punto en donde puede considerarse aplicada la fuerza de empuje. Ello significa que las fuerzas E y P forman un par que hará girar el cuerpo hasta que ambas estén alineadas.
Equilibrio de los cuerpos flotantes
Si un cuerpo sumergido sale a flote es porque el empuje predomina sobre el peso (E >P). En el equilibrio ambas fuerzas aplicadas sobre puntos diferentes estarán alineadas; tal es el caso de las embarcaciones en aguas tranquilas, por ejemplo. Si por efecto de una fuerza lateral, como la producida por un golpe de mar, el eje vertical del navío se inclinara hacia un lado, aparecerá un par de fuerzas que harán oscilar el barco de un lado a otro. Cuanto mayor sea el momento M del par, mayor será la estabilidad del navío, es decir, la capacidad para recuperar la verticalidad. Ello se consigue diseñando convenientemente el casco y repartiendo la carga de modo que rebaje la posición del centro de gravedad, con lo que se consigue aumentar el brazo del par.
"Fisicanet dixit"
Definiciones sobre Presión
El concepto de presión
Cuando se ejerce una fuerza sobre un cuerpo deformable, los efectos que provoca dependen no sólo de su intensidad, sino también de cómo esté repartida sobre la superficie del cuerpo. Así, un golpe de martillo sobre un clavo bien afilado hace que penetre mas en la pared de lo que lo haría otro clavo sin punta que recibiera el mismo impacto. Un individuo situado de puntillas sobre una capa de nieve blanda se hunde, en tanto que otro de igual peso que calce raquetas, al repartir la fuerza sobre una mayor superficie, puede caminar sin dificultad. El cociente entre la intensidad F de la fuerza aplicada perpendicularmente sobre una superficie dada y el área S de dicha superficie se denomina presión:
p = F/S
La presión representa la intensidad de la fuerza que se ejerce sobre cada unidad de área de la superficie considerada. Cuanto mayor sea la fuerza que actúa sobre una superficie dada, mayor será la presión, y cuanto menor sea la superficie para una fuerza dada, mayor será entonces la presión resultante.
La presión en los fluidos
El concepto de presión es muy general y por ello puede emplearse siempre que exista una fuerza actuando sobre una superficie. Sin embargo, su empleo resulta especialmente útil cuando el cuerpo o sistema sobre el que se ejercen las fuerzas es deformable. Los fluidos no tienen forma propia y constituyen el principal ejemplo de aquellos casos en los que es más adecuado utilizar el concepto de presión que el de fuerza.
Cuando un fluido está contenido en un recipiente, ejerce una fuerza sobre sus paredes y, por tanto, puede hablarse también de presión. Si el fluido está en equilibrio las fuerzas sobre las paredes son perpendiculares a cada porción de superficie del recipiente, ya que de no serlo existirían componentes paralelas que provocarían el desplazamiento de la masa de fluido en contra de la hipótesis de equilibrio. La orientación de la superficie determina la dirección de la fuerza de presión, por lo que el cociente de ambas, que es precisamente la presión, resulta independiente de la dirección; se trata entonces de una magnitud escalar.
Unidades de presión
En el SI la unidad de presión es el pascal, se representa por Pa y se define como la presión correspondiente a una fuerza de un newton de intensidad actuando perpendicularmente sobre una superficie plana de un metro cuadrado. 1 Pa equivale, por tanto, a 1 N/m ².
Existen, no obstante, otras unidades de presión que sin corresponder a ningún sistema de unidades en particular han sido consagradas por el uso y se siguen usando en la actualidad junto con el pascal. Entre ellas se encuentran la atmósfera y el bar.
La atmósfera (atmósfera) se define como la presión que a 0 °C ejercería el peso de una columna de mercurio de 76 cm de altura y 1 cm ² de sección sobre su base. Es posible calcular su equivalencia en N/m ² sabiendo que la densidad del mercurio es igual a 13,6.10³ kg/m ³ y recurriendo a las siguientes relaciones entre magnitudes:
Peso (N) = masa (kg).9,8 m/s ²
Masa = volumen.densidad
Presión = Fuerza / Superficie
Como el volumen del cilindro que forma la columna es igual a la superficie de la base por la altura, se tendrá:
Presión = 1 atmósfera = masa.9,8 m/s ²/superficie = superficie.(0,76 m.13,6.10³ kg/m ³.9,8 m/s ²)/superficie
es decir: 1 atmósfera = 1,013.105 Pa.
El bar es realmente un múltiple del pascal y equivale a 105 N/m ². En meteorología se emplea con frecuencia el milibar (mb) o milésima parte del bar 1 mb = 10 ² Pa y 1 atmósfera = 1.013 mb
LA HIDROSTATICA
La ecuación fundamental de la hidrostática
Todos los líquidos pesan, por ello cuando están contenidos en un recipiente las capas superiores oprimen a las inferiores, generándose una presión debida al peso. La presión en un punto determinado del líquido deberá depender entonces de la altura de la columna de líquido que tenga por encima suyo. Considérese un punto cualquiera del líquido que diste una altura h de la superficie libre de dicho líquido. La fuerza del peso debido a una columna cilíndrica de líquido de base S situada sobre él puede expresarse en la forma
F peso = mg = V.g = g.h.S
siendo V el volumen de la columna y δ la densidad del líquido, la presión debida al peso vendrá dada por:
p peso = F/A = g.h.S/S = h.δ.g
La presión en un punto
La definición de la presión como cociente entre la fuerza y la superficie se refiere a una fuerza constante que actúa perpendicularmente sobre una superficie plana. En los líquidos en equilibrio las fuerzas asociadas a la presión son en cada punto perpendiculares a la superficie del recipiente, de ahí que la presión sea considerada como una magnitud escalar cociente de dos magnitudes vectoriales de igual dirección: la fuerza y el vector superficie. Dicho vector tiene por módulo el área y por dirección la perpendicular a la superficie.
Cuando la fuerza no es constante, sino que varía de un punto a otro de la superficie S considerada, tiene sentido hablar de la presión en un punto dado. Si la fuerza es variable y F representa la resultante de todas las fuerzas que actúan sobre la superficie S la fórmula
p = F/S
define, en este caso, la presión media. Si sobre la superficie libre se ejerciera una presión exterior adicional po,como la atmosférica por ejemplo, la presión total p en el punto de altura h sería:
p = p0 + p peso = p0 + h.δ.g
Esta ecuación puede generalizarse al caso de que se trate de calcular la diferencia de presiones Δ p entre dos puntos cualesquiera del interior del líquido situados a diferentes alturas,resultando:
δ p = δ.g.δ h
es decir:
p2 - p1 = δ.g.(h2 - h1)
que constituye la llamada ecuación fundamental de la hidrostática. Esta ecuación indica que para un líquido dado y para una presión exterior constante la presión en el interior depende únicamente de la altura. Por tanto, todos los puntos del líquido que se encuentren al mismo nivel soportan igual presión. Ello implica que ni la forma de un recipiente ni la cantidad de líquido que contiene influyen en la presión que se ejerce sobre su fondo, tan sólo la altura de líquido. Esto es lo que se conoce como paradoja hidrostática, cuya explicación se deduce a modo de consecuencia de la ecuación fundamental.
El principio de Pascal y sus aplicaciones
La presión aplicada en un punto de un líquido contenido en un recipiente se transmite con el mismo valor a cada una de las partes del mismo. Este enunciado, obtenido a partir de observaciones y experimentos por el físico y matemático francés Blaise Pascal (1623-1662), se conoce como principio de Pascal.
El principio de Pascal puede ser interpretado como una consecuencia de la ecuación fundamental de la hidrostática y del carácter incompresible de los líquidos. En esta clase de fluidos la densidad es constante, de modo que de acuerdo con la ecuación p = p0 + ρ . g.h si se aumenta la presión en la superficie libre, por ejemplo, la presión en el fondo ha de aumentar en la misma medida, ya que ρ . g.h no varía al no hacerlo h.
La prensa hidráulica constituye la aplicación fundamental del principio de Pascal y también un dispositivo que permite entender mejor su significado.
Consiste, en esencia, en dos cilindros de diferente sección comunicados entre sí, y cuyo interior está completamente lleno de un líquido que puede ser agua o aceite. Dos émbolos de secciones diferentes se ajustan, respectivamente, en cada uno de los dos cilindros, de modo que estén en contacto con el líquido. Cuando sobre el émbolo de menor sección S1 se ejerce una fuerza F1 la presión p1 que se origina en el líquido en contacto con él se transmite íntegramente y de forma instantánea a todo el resto del líquido; por tanto, será igual a la presión p2 que ejerce el líquido sobre el émbolo de mayor sección S2, es decir:
p1 = p2 F1/S1 = F2/S2 F1 = F2.S1/S2
Si la sección S2 es veinte veces mayor que la S1, la fuerza F1 aplicada sobre el émbolo pequeño se ve multiplicada por veinte en el émbolo grande. La prensa hidráulica es una máquina simple semejante a la palanca de Arquímedes, que permite amplificar la intensidad de las fuerzas y constituye el fundamento de elevadores, prensas, frenos y muchos otros dispositivos hidráulicos de maquinaria industrial.
Cuando se ejerce una fuerza sobre un cuerpo deformable, los efectos que provoca dependen no sólo de su intensidad, sino también de cómo esté repartida sobre la superficie del cuerpo. Así, un golpe de martillo sobre un clavo bien afilado hace que penetre mas en la pared de lo que lo haría otro clavo sin punta que recibiera el mismo impacto. Un individuo situado de puntillas sobre una capa de nieve blanda se hunde, en tanto que otro de igual peso que calce raquetas, al repartir la fuerza sobre una mayor superficie, puede caminar sin dificultad. El cociente entre la intensidad F de la fuerza aplicada perpendicularmente sobre una superficie dada y el área S de dicha superficie se denomina presión:
p = F/S
La presión representa la intensidad de la fuerza que se ejerce sobre cada unidad de área de la superficie considerada. Cuanto mayor sea la fuerza que actúa sobre una superficie dada, mayor será la presión, y cuanto menor sea la superficie para una fuerza dada, mayor será entonces la presión resultante.
La presión en los fluidos
El concepto de presión es muy general y por ello puede emplearse siempre que exista una fuerza actuando sobre una superficie. Sin embargo, su empleo resulta especialmente útil cuando el cuerpo o sistema sobre el que se ejercen las fuerzas es deformable. Los fluidos no tienen forma propia y constituyen el principal ejemplo de aquellos casos en los que es más adecuado utilizar el concepto de presión que el de fuerza.
Cuando un fluido está contenido en un recipiente, ejerce una fuerza sobre sus paredes y, por tanto, puede hablarse también de presión. Si el fluido está en equilibrio las fuerzas sobre las paredes son perpendiculares a cada porción de superficie del recipiente, ya que de no serlo existirían componentes paralelas que provocarían el desplazamiento de la masa de fluido en contra de la hipótesis de equilibrio. La orientación de la superficie determina la dirección de la fuerza de presión, por lo que el cociente de ambas, que es precisamente la presión, resulta independiente de la dirección; se trata entonces de una magnitud escalar.
Unidades de presión
En el SI la unidad de presión es el pascal, se representa por Pa y se define como la presión correspondiente a una fuerza de un newton de intensidad actuando perpendicularmente sobre una superficie plana de un metro cuadrado. 1 Pa equivale, por tanto, a 1 N/m ².
Existen, no obstante, otras unidades de presión que sin corresponder a ningún sistema de unidades en particular han sido consagradas por el uso y se siguen usando en la actualidad junto con el pascal. Entre ellas se encuentran la atmósfera y el bar.
La atmósfera (atmósfera) se define como la presión que a 0 °C ejercería el peso de una columna de mercurio de 76 cm de altura y 1 cm ² de sección sobre su base. Es posible calcular su equivalencia en N/m ² sabiendo que la densidad del mercurio es igual a 13,6.10³ kg/m ³ y recurriendo a las siguientes relaciones entre magnitudes:
Peso (N) = masa (kg).9,8 m/s ²
Masa = volumen.densidad
Presión = Fuerza / Superficie
Como el volumen del cilindro que forma la columna es igual a la superficie de la base por la altura, se tendrá:
Presión = 1 atmósfera = masa.9,8 m/s ²/superficie = superficie.(0,76 m.13,6.10³ kg/m ³.9,8 m/s ²)/superficie
es decir: 1 atmósfera = 1,013.105 Pa.
El bar es realmente un múltiple del pascal y equivale a 105 N/m ². En meteorología se emplea con frecuencia el milibar (mb) o milésima parte del bar 1 mb = 10 ² Pa y 1 atmósfera = 1.013 mb
LA HIDROSTATICA
La ecuación fundamental de la hidrostática
Todos los líquidos pesan, por ello cuando están contenidos en un recipiente las capas superiores oprimen a las inferiores, generándose una presión debida al peso. La presión en un punto determinado del líquido deberá depender entonces de la altura de la columna de líquido que tenga por encima suyo. Considérese un punto cualquiera del líquido que diste una altura h de la superficie libre de dicho líquido. La fuerza del peso debido a una columna cilíndrica de líquido de base S situada sobre él puede expresarse en la forma
F peso = mg = V.g = g.h.S
siendo V el volumen de la columna y δ la densidad del líquido, la presión debida al peso vendrá dada por:
p peso = F/A = g.h.S/S = h.δ.g
La presión en un punto
La definición de la presión como cociente entre la fuerza y la superficie se refiere a una fuerza constante que actúa perpendicularmente sobre una superficie plana. En los líquidos en equilibrio las fuerzas asociadas a la presión son en cada punto perpendiculares a la superficie del recipiente, de ahí que la presión sea considerada como una magnitud escalar cociente de dos magnitudes vectoriales de igual dirección: la fuerza y el vector superficie. Dicho vector tiene por módulo el área y por dirección la perpendicular a la superficie.
Cuando la fuerza no es constante, sino que varía de un punto a otro de la superficie S considerada, tiene sentido hablar de la presión en un punto dado. Si la fuerza es variable y F representa la resultante de todas las fuerzas que actúan sobre la superficie S la fórmula
p = F/S
define, en este caso, la presión media. Si sobre la superficie libre se ejerciera una presión exterior adicional po,como la atmosférica por ejemplo, la presión total p en el punto de altura h sería:
p = p0 + p peso = p0 + h.δ.g
Esta ecuación puede generalizarse al caso de que se trate de calcular la diferencia de presiones Δ p entre dos puntos cualesquiera del interior del líquido situados a diferentes alturas,resultando:
δ p = δ.g.δ h
es decir:
p2 - p1 = δ.g.(h2 - h1)
que constituye la llamada ecuación fundamental de la hidrostática. Esta ecuación indica que para un líquido dado y para una presión exterior constante la presión en el interior depende únicamente de la altura. Por tanto, todos los puntos del líquido que se encuentren al mismo nivel soportan igual presión. Ello implica que ni la forma de un recipiente ni la cantidad de líquido que contiene influyen en la presión que se ejerce sobre su fondo, tan sólo la altura de líquido. Esto es lo que se conoce como paradoja hidrostática, cuya explicación se deduce a modo de consecuencia de la ecuación fundamental.
El principio de Pascal y sus aplicaciones
La presión aplicada en un punto de un líquido contenido en un recipiente se transmite con el mismo valor a cada una de las partes del mismo. Este enunciado, obtenido a partir de observaciones y experimentos por el físico y matemático francés Blaise Pascal (1623-1662), se conoce como principio de Pascal.
El principio de Pascal puede ser interpretado como una consecuencia de la ecuación fundamental de la hidrostática y del carácter incompresible de los líquidos. En esta clase de fluidos la densidad es constante, de modo que de acuerdo con la ecuación p = p0 + ρ . g.h si se aumenta la presión en la superficie libre, por ejemplo, la presión en el fondo ha de aumentar en la misma medida, ya que ρ . g.h no varía al no hacerlo h.
La prensa hidráulica constituye la aplicación fundamental del principio de Pascal y también un dispositivo que permite entender mejor su significado.
Consiste, en esencia, en dos cilindros de diferente sección comunicados entre sí, y cuyo interior está completamente lleno de un líquido que puede ser agua o aceite. Dos émbolos de secciones diferentes se ajustan, respectivamente, en cada uno de los dos cilindros, de modo que estén en contacto con el líquido. Cuando sobre el émbolo de menor sección S1 se ejerce una fuerza F1 la presión p1 que se origina en el líquido en contacto con él se transmite íntegramente y de forma instantánea a todo el resto del líquido; por tanto, será igual a la presión p2 que ejerce el líquido sobre el émbolo de mayor sección S2, es decir:
p1 = p2 F1/S1 = F2/S2 F1 = F2.S1/S2
Si la sección S2 es veinte veces mayor que la S1, la fuerza F1 aplicada sobre el émbolo pequeño se ve multiplicada por veinte en el émbolo grande. La prensa hidráulica es una máquina simple semejante a la palanca de Arquímedes, que permite amplificar la intensidad de las fuerzas y constituye el fundamento de elevadores, prensas, frenos y muchos otros dispositivos hidráulicos de maquinaria industrial.
Suscribirse a:
Comentarios (Atom)
